Система понятий о веществе состоит из следующих компонентов: 1) состав веществ; 2) строение; 3) свойства; 4) классификация; 5) получение; 6) химические методы исследования; 7) применение. Ограничиваться выделением лишь известного "треугольника": состав—строение—свойства — для целей обучения недостаточно, несмотря на его ведущую роль.
Структура системы понятий о классификации веществ
Классификацию веществ (схема 1) нельзя дать только на основе какого-то одного критерия
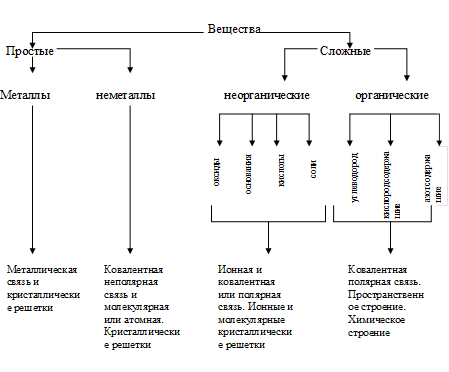
Схема 1 Система понятий о классификации веществ
Это сильно обеднит представления учащихся о веществе. Так, например, неорганические вещества учащиеся классифицируют вначале по составу. После изучения электронного строения вещества появляется новый принцип классификации веществ по строению вещества — по видам химической связи и по типам кристаллической решетки. Этот принцип классификации веществ получает свое развитие в темах "Теория электролитической диссоциации", где разбирается донорно-акцепторный механизм ковалентной связи, а также в теме "Металлы", где изучаются металлическая связь и металлическая кристаллическая решетка.
При рассмотрении теории электролитической диссоциации вещества классифицируют по свойствам в растворах и соединениях. Далее при изучении поведения в окислительно-восстановительных реакциях вещества разделяют на окислители и восстановители.
В органической химии вначале классификация осуществляется по составу на три большие группы: углеводороды, кислородсодержание и азотсодержание, а внутри их — по строению (схема 2).
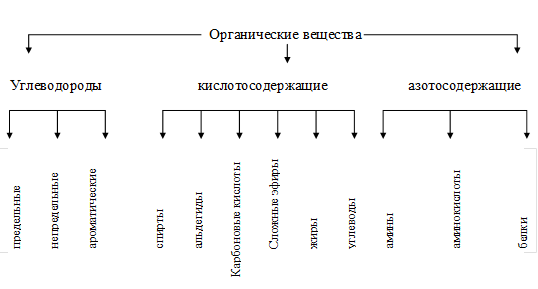
Схема 2 Классификация органических веществ
Таким образом, главными критериями классификации веществ является их состав и строение. Деление веществ по свойствам на окислители и восстановители, а также на электролиты и неэлектролиты является, во-первых, относительным, а во-вторых, функцией состава и строения веществ.
Понятия о классификации веществ позволяют устанавливать связи между веществами разных групп, подчеркивают идею материального единства мира [5, 159].
Свойства веществ систематизируют исходя из их состава или строения. Связи эти причинно-следственные.
Формирование системы понятий о веществе начинается с самых первых уроков на основе межпредметных связей с физикой. Определение вещества не дают, разъясняют только смысл понятия о веществе в сопоставлении с уже известным учащимся из физики понятием о теле и говорят о том, что каждое вещество имеет свои свойства. Но поскольку тела могут состоять из разных веществ, дается понятие о смеси веществ и о чистом веществе и сразу же включается понятие о методах исследования, например способах очистки веществ. Понятие о молекуле используется то, что было получено на уроках физики. Затем вводится первое понятие о классификации веществ на простые и сложные и их определение. Почти сразу дается понятие о количественной характеристике вещества — о их относительной молекулярной массе, о постоянстве их состава [13, 177].
В теме "Кислород. Оксиды. Горение" приводятся состав простого вещества кислорода, его свойства, методы, исследования свойств посредством химического эксперимента (получение из перманганата калия). В этой теме вводится новое понятие о кислороде как окислителе. Понятия о строении вещества в этой теме дальнейшего развития не получают.
В теме "Кислород. Оксиды. Горение" развивается понятие о сложных веществах — оксидах. Рассматриваются их состав и некоторые свойства, в частности свойство оксида углерода (IV) вызывать помутнение известковой воды, свойство оксида фосфора (V) растворяться в воде, получение оксидов при взаимодействии кислорода с простыми и сложными веществами. Но все это пока лишь внешнее описание без объяснения сущности — накопление фактов.
В теме "Кислород. Оксиды. Горение" развивается понятие о смеси веществ на примере воздуха, дальнейшая его конкретизация — в теме "Водород. Кислоты. Соли". Понятие обогащается новым конкретным содержанием: вещество — восстановитель. Осторожно и очень медленно, чтобы избежать формального усвоения, вводят понятие о кислотах:
1) сначала учащимся рассказывают о кислотах, известных им из практики, — лимонной, яблочной, щавелевой, молочной, муравьиной, уксусной, отмечают их кислый вкус, иногда едкость, жгучесть (муравьиная кислота);
2) затем демонстрируют осушающее действие серной кислоты, ее разогревание при растворении, обугливание органических веществ. Обсуждают правила техники безопасности при работе с серной кислотой;
3) далее переходят к общим свойствам соляной кислоты (дымящая): действие на индикаторы (объясняется слово "индикатор"), на металлы;
4) состав кислот — абстрактный материал. Учащихся знакомят с формулами четырех кислот: НСl, НNО3, Н2SО4, Н3РO4. Это примеры для классификации по составу и по основности. Так накапливается материал для классификации.
В органической химии система понятий о строении вещества обогащается таким большим числом качественно новых знаний, что актуализация предшествующих опорных знаний становится обязательным условием усвоения учащимися содержания органической химии.
Понятия химического строения: химическое строение как порядок соединения и взаимного влияния атомов в молекулах, изомерия, гомология.
Понятия пространственного строения — более высокий этап познания строения по отношению к химическому строению. Имеются в виду понятия о валентных углах и геометрии молекул органических веществ.
Особое внимание в органической химии уделяется энергетическим характеристикам веществ, в частности энергии связи.
Вопросы химического, электронного, стереохимического строения органических веществ, энергетические представления получают такое мощное развитие, что обособляются в отдельную теорию.
Структура содержания понятия "химический элемент". Как и всякое сложное понятие, система понятий "химический элемент" имеет свою структуру содержания. В состав ее входят понятия: 1) об атомах химических элементов; 2) о распространенности и круговороте элементов в природе; 3) о классификации и систематизации химических элементов. Все три блока тесно связаны между собой, а кроме того, и с понятием "вещество".
Каждый из указанных блоков содержания имеет свою структуру. Например, понятия об атомах можно сгруппировать так: строение атомов, свойства атомов. Они связаны между собой причинно-следственной связью (схема 3).
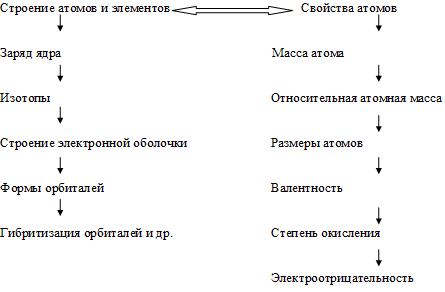
Схема 3 Причинно-следственная связь
Выявление этой связи в каждом конкретном случае позволяет организовать проблемные ситуации. Например, объяснение связи между строением электронной оболочки атома и его степенью окисления позволяет построить цепочку умозаключений по прогнозированию возможных степеней окисления. (Строение атома серы позволяет предположить, что отрицательная степень окисления ее должна быть равна -2, а высшая положительная +6. Дальнейшее рассуждение позволит прогнозировать свойства веществ, содержащих серу в соответствующей степени окисления.) Легко просматривается связь между числом электронных слоев и радиусом атома, строением электронной оболочки и электроотрицательностью. Интересно выявление и обратных связей, когда требуется установить строение внешнего электронного слоя на основании известных степеней окисления.
Вполне понятно, что формирование системы понятий о химическом элементе происходит не сразу, а постепенно, последовательно, обогащаясь за счет изучаемых в процессе обучения теорий. Начинается оно с формирования понятий об атоме.
Формирование понятий о естественных группах сходных элементов. Знакомя всех учащихся с понятием об естественных группах сходных химических элементов, вначале употребляют термин "естественное семейство", чтобы не путать его с группами периодической системы. Формируют это понятие индуктивным путем на трех семействах — благородных газах, щелочных металлах и галогенах. Подход к ним единый: составление сводной таблицы по каждому семейству с соотнесением свойств с относительной атомной массой. Используют разные приемы, например таблицы, отражающие сравнительную характеристику галогенов, щелочных металлов и др.
Таблица 1 Сравнительная характеристика галогенов
| Элемент | Химический знак | Относительная атомная масса | Формула простого вещества | Физическое состояние | Окраска | Плотность | Температура кипения | Растворимость в воде |
Таблица 2 Сравнительная характеристика щелочей
| Элемент | Химический знак | Валентность в кислородных соединениях | Условия реакции с кислородом | Валентность в летучих водородных соединениях | Условия реакции с водородом |
Таблица 3 Сравнительная характеристика гидроксидов
| Элемент | Химический знак | Формула высшего оксида | Характер свойств оксида | Формула высшего гидроксида | Характер свойств гидроксида | Формула летучего водородного соединения |
В процессе сравнения используют химический эксперимент и другие средства наглядности. В результате делают выводы по следующим параметрам:
1) сходство свойств между элементами изучаемого семейства;
2) различие свойств изучаемого семейства;
3) взаимосвязь свойств и значений атомной массы;
4) сходство и различие свойств семейств и их зависимость от значения атомной массы.
Последний пункт особенно важен для понимания периодического закона. Все это необходимый фактический материал, не получающий пока теоретического объяснения, так как учащиеся пока еще не знакомы со строением атомов. Естественно, возникает проблемная ситуация, которая будет решаться на последующих уроках. Она состоит в противоречии между необходимостью объяснения фактов и нехваткой имеющихся знаний. Учитель должен эту проблему вскрыть и четко ее сформулировать: почему наблюдается такая закономерность в изменениях свойств в зависимости от атомных масс элементов?
Затем при изучении периодического закона и периодической системы элементов Д. И. Менделеева происходит качественный скачок в развитии понятий об атомах. Атом предстает как сложная система, состоящая из ядра и электронной оболочки. Здесь дается понятие об изотопах [5, 35].
Значительно пополняются представления учащихся о свойствах атомов. Вводятся представления об атомном радиусе, о степени окисления, электроотрицательности. Понятие "степень окисления" при всей его условности методически очень важно, так как помогает раскрыть сущность периодичности, облегчает пользование периодической системой. На этой стадии следует разграничить понятия "степень окисления" и "валентность" чтобы в дальнейшем учащиеся их четко различали.
Особое внимание при формировании системы понятий о химическом элементе следует обратить на тему "Обобщение знаний по курсу неорганической химии". Здесь устанавливаются внутрипредметные связи между важнейшими химическими понятиями — о химическом элементе, веществе, химической реакции и химическом производстве. Эта тема очень важна для формирования у учащихся правильных теоретических представлений о соотношении этих понятий. Она является отправной точкой, подготавливающей переход от неорганической к органической химии. После нее значительно легче сопоставлять и сравнивать свойства органических веществ с неорганическими, выявлять особенности органических реакций по сравнению с неорганическими. Формирование системы понятий о химическом элементе завершается в основном именно в этой теме [9, 50].
Таким образом, развитие понятия "химический элемент" осуществляется в несколько этапов:
1) подготовительный — до формулирования определения химического элемента;
2) экспериментальный — до изучения атомно-молекулярного учения;
3) изучение элементов на базе атомно-молекулярного учения;
4) формирование понятия о естественной группе элементов;
5) изучение периодической системы Д. И. Менделеева и теории строения атома;
6) изучение элементов по группам периодической системы;
7) обобщение знаний учащихся в конце IX класса, установление связей понятия о химическом элементе с другими понятиями курса химии.
В X классе завершается развитие понятия о химическом элементе. В курсе органической химии прежде всего отмечают, что молекулы органических веществ состоят из атомов тех же элементов, что и неорганических.
Далее рассматривается понятие о гибридизации орбиталей атома углерода, а также о том, что атомы элемента в составе соединения не просто суммируются в разных комбинациях, а испытывают влияние других атомов, т. е. атомы одного и того же элемента в разных соединениях несколько отличаются друг от друга по свойствам. Эту мысль можно провести и в неорганической химии, но в органической она звучит более убедительно.
В курсе органической химии дается понятие о возможности соединения в одном и том же веществе большого числа одноименных атомов, что редко наблюдается в неорганических веществах.
В конце курса X класса в обобщающей теме понятие об элементе должно прозвучать как важнейшее связующее звено между неорганической и органической химией. Поэтому заключительное обобщение начинается именно с него. Особое внимание обращают на философский смысл и воспитательное значение учения о химических элементах.
Структура системы понятий о химической реакции. Понятие о химической реакции сложное и многогранное. Это, как и понятие "вещество", целая система понятий, имеющая свою структуру. В курсе химии средней школы четко различаются шесть компонентов понятия "химическая реакция", которые рассматриваются в единстве и формируются постепенно:
1) признаки, сущность и механизм реакций; 2) закономерности возникновения и протекания; 3) количественные характеристики; 4) классификация; 5) практическое использование; 6) методы исследования. Сочетание этих шести блоков понятий не только определяет систему знаний, но и позволяет вскрыть философскую сущность понятия "химическая реакция". Химическая реакция должна характеризоваться с позиций всех шести блоков содержания понятия. Каждый из них имеет свою структуру. Например, структура содержания понятий о классификации химических реакций имеет такой вид (табл. 4).
Таблица 4 Классификация химических реакций
| Принципы классификации | Характеристика реакций | Примеры реакций |
| Исходное состояние реагирующей системы | Гомогенные Гетерогенные | Взаимодействие азота с кислородом Взаимодействие оксида кальция с оксидом углерода (IV) |
| Наличие окислительно-восстановительного процесса | Окислительно-восстановительные Реакции, в которых окислительно-восстановительный процесс отсутствует | Взаимодействие цинка с соляной кислотой Разложение карбоната кальция с образованием оксида кальция и оксида углерода (IV) |
| Участие катализатора | Каталитические Некаталитические | Взаимодействие азота с водородом Взаимодействие оксида серы (IV) с водой |
| Обратимость реакции | Обратимые Необратимые | Взаимодействие оксида серы (IV) с водой Разложение дихромата аммония |
| Энергетический эффект реакции | Экзотермические Эндотермические | Горение магния Разложение оксида ртути |
| Соотношение числа исходных и полученных веществ | Соединение Разложение Замещение и обмен | Взаимодействие оксида кальция с водой Разложение оксида ртути Взаимодействие железа и хлорида меди (II) Взаимодействие нитрата серебра и хлорида натрия |
| Реакции, протекающие без изменения качественного состава простых и сложных веществ | Аллотропные превращения Изомеризация | Превращение кислорода в озон Образование одного изомера из другого |
Такими должны быть знания учащихся о классификации химических реакций после усвоения школьного курса химии.
Система понятий о сущности, механизмах и признаках химической реакции может быть представлена двумя сторонами: понятиями о внешних признаках и внутренней сущности реакций. Между ними существует причинно-следственная связь [2, 29].
Понятие о внутренней сущности реакций развивается постепенно, усложняясь при переходе от теории к теории. В атомно-молекулярном учении сущность химической реакции объясняется как перегруппировка атомов. При изучении электронного строения веществ химические реакции рассматриваются как процесс разрыва одних связей и образование других, на уровне теории электролитической диссоциации — как взаимодействие ионов, а при изучении теории строения органических веществ анализируется механизм протекания химической реакции.
Последовательность формирования понятия "химическая реакция". Понятие "химическая реакция" формируется на нескольких уровнях.
Уровень 1. Понятие о химической реакции начинается формироваться с самых первых уроков. Сначала дают понятие о химическом явлении, так как термин "явление" более знаком учащимся, а затем сообщают, что химическое явление — это и есть химическая реакция. На этом этапе опора делается на знания, полученные учащимися из физики. На уровне атомно-молекулярного учения разъясняют, как можно по внешним признакам обнаружить химическую реакцию (образование осадка, изменение окраски, выделение газа, выделение или поглощение теплоты и т. д.) [7, 169].
Классификация химических реакций дается на уровне сравнения числа исходных и полученных веществ. При этом учащиеся используют такие мыслительные приемы: сравнение, анализ, синтез, обобщение. Все эти сведения о химической реакции включены в тему "Первоначальные химические понятия". Далее все стороны системы понятий о химической реакции должны расширяться и дополняться новыми данными, т. е. после этапа обобщения снова начинается этап накопления.
В теме "Кислород. Оксиды. Горение" понятие о химической реакции обогащается новыми фактами, вводится частное понятие об окислении, но уровень объяснений и обоснований тот же, что и в предыдущей теме. Такой индуктивный логический подход применяется тогда, когда для широких обобщений нет еще подготовки. Здесь говорится об окислении как химической реакции, но рассматривается оно как соединение с кислородом, т. е. применяется изученный учащимися принцип классификации.
Закономерности протекания реакций разбираются при изучении условий возникновения и прекращения горения. Новым здесь является понятие о катализаторе на примере бертолетовой соли и первые, самые простые, представления о скорости химической реакции. Впервые вопрос о скорости химической реакции затрагивается в теме "Вода. Растворы. Основания", и возвращаются к нему только в конце IХ класса при изучении темы "Основные закономерности химических реакций. Производство серной кислоты".
В темах "Водород. Кислоты. Соли", "Вода. Растворы. Основания" понятие о химической реакции обогащается фактическим материалом. Дается понятие о реакции обмена на примерах взаимодействия кислот с оксидами, о реакции нейтрализации кислоты основанием, о восстановлении как разновидности реакции замещения и как о процессе отнятия кислорода от вещества.
Уровень 2. В теме VIII класса "Количественные отношения в химии" понятие о химической реакции получает дальнейшее развитие. В частности, начинают формироваться энергетические представления о химических процессах. Рассматривается понятие об экзотермических и эндотермических реакциях, вводится качественно новое понятие о тепловом эффекте химических реакций, термохимических уравнениях. Именно здесь раскрывается на химическом материале важнейший закон природы — закон сохранения и превращения энергии. Так появляется возможность снова показать, что все химические процессы имеют две стороны — качественную и количественную. При изучении энергетики химической реакции учитель обязательно должен установить межпредметную связь с физикой на основе закона сохранения и превращения энергии. Это создаст условия для формирования научно-материалистического мировоззрения, утверждения идеи о материальном единстве мира и даст возможность упомянуть о новой форме энергии — энергии, выделяемой при химических реакциях. В этой теме количественные отношения веществ трактуются как молярные отношения реагирующих веществ и продуктов реакции. С помощью соответствующего перерасчета эти отношения можно выразить как массовые или объемные отношения (если речь идет о газах).
Уровень 3. Понятие о химической реакции претерпевает качественное изменение в теме "Химическая связь. Строение вещества". Химическая реакция начинает трактоваться как разрушение одних связей и образование новых. Рассматривается это на примере окислительно-восстановительных реакций. Механизм реакции окисления и восстановления объясняют с точки зрения перехода электронов, поднимаясь на более высокий теоретический уровень. На основе нового понятия "степень окисления" анализируют известные учащимся реакции разных типов, доказывая, что среди реакций любого типа можно найти окислительно-восстановительные. Следовательно, степень окисления элемента — это, как правило, еще один критерий классификации химических реакций. Здесь появляется возможность показать учащимся диалектический характер окислительно-восстановительных процессов (единство и борьба противоположностей).
В теме "Галогены" дается первое понятие о качественной реакции на примере соляной кислоты и хлоридов. В теме "Подгруппа кислорода" вводится новый тип реакций — аллотропные превращения на примере озона, серы.
Уровень 4. Наибольшее развитие понятия о закономерностях протекания химических реакций получат в теме "Основные закономерности химических реакций. Производство серной кислоты". Здесь дают понятие о скорости химической реакции и о факторах, влияющих на скорость (природа реагирующих веществ, их концентрация, поверхность соприкосновения, температура, наличие катализатора), приводится формула прямой зависимости скорости от концентрации реагирующих веществ, говорится о температурном коэффициенте скорости.
В этой теме развивается и обобщается понятие о химической реакции.
Уровень 5. Тема "Теория электролитической диссоциации", с которой начинается курс химии в IX классе, помимо мировоззренческого значения, вносит много нового в объяснение механизма реакции. На базе понятия об обратимости реакций можно объяснить сущность процесса диссоциации, а также гидролиза солей. Гидролиз рассматривается только в ионной форме, чтобы не вводить понятие о гидроксо-солях. Гидролиз — очень важное теоретическое понятие, которое развивается в последующих темах IX класса и в органической химии. Его следует изучать с использованием понятия о химическом равновесии.
Далее изучение химических реакций в IX классе происходит дедуктивно. Знания, сформированные на базе перечисленных теорий, применяются для объяснения фактов и явлений и прогнозирования протекания процессов.
Уровень 6. Дальнейшее развитие понятия "химическая реакция" осуществляется в курсе органической химии. Понятие о классификации химических реакций дополняется и расширяется. В курсе органической химии вводится новый тип реакции — изомеризация. Самая первая классификация реакций на типы приобретает качественно новое, более глубокое содержание. Например, реакция замещения — галогенирование алканов приводит не к образованию нового простого и нового сложного вещества, а к образованию двух сложных веществ. Реакция соединения включает в себя целую систему понятий органического синтеза: гидрирование, гидратацию, полимеризацию, фотосинтез и др. Реакция разложения объединяет такую систему понятий, как крекинг, риформинг, гидролиз (омыление) и т. д.
В органической химии вносится качественно новый материал в понятия и о механизмах реакций [38, 144]. Впервые дается представление о свободнорадикальном механизме реакций замещения и полимеризации и ионном механизме реакций присоединения. Свободнорадикальный механизм рассматривают на примере реакций замещения (галогенирование алканов), присоединения (полимеризация), отщепления (крекинг углеводородов). В неорганической химии этот механизм не разбирают (цепные реакции исключены из программы). Расширяется понятие о ионном механизме химической реакции: приводятся примеры присоединения неорганических веществ к алкенам (симметричным и несимметричным), реакций замещения при гидролизе гало-геноалкилов.
Уровень 7. В теме "Обобщение знаний по неорганической и органической химии" завершается обобщение понятия "химическая реакция". В конце обучения учащийся должен суметь охарактеризовать предложенную ему в качестве примера химическую реакцию в свете компонентов содержания [16, 134].
Дата: 2019-07-31, просмотров: 464.