На включение одной аминокислоты в растущую полипептидную цепь клетка затрачивает 4 макроэргические связи: 2 из АТФ в ходе реакции, катализируемой аа-тРНК синтетазой (в процессе активации аминокислот АТФ расщепляется на АМФ и пирофосфат), и 2 молекулы ГТФ: одна используется на связывание аа-тРНК в А-центре рибосомы, а вторая затрачивается на стадию транслокации. К этому |следует добавить использование ещё двух макроэргических связей молекул: АТФ и ГТФ на инициацию и терминацию синтеза полипептидной цепи.
Этапы синтеза полипептидной цепи
Синтез белка представляет собой циклический многоступенчатый энергозависимый процесс, в котором свободные аминокислоты полимеризуется в генетически детерминированную последовательность с образованием полипептидов. Система белкового синтеза, точнее система трансляции, которая использует генетическую информацию, транскрибированную в мРНК, для синтеза полипептидной цепи с определенной первичной структурой, включает около 200 типов макромолекул – белков и нуклеиновых кислот. Среди них около 100 макромолекул, участвующих в активировании аминокислот и их переносе на рибосомы, более 60 макромолекул, входящих в состав 70S или 80S рибосом, и около 10S макромолекул, принимающих непосредственное участие в системе трансляции. Не разбирая природу других важных для синтеза факторов, рассмотрим подробно механизм индивидуальных путей синтеза белковой молекулы в искусственной синтезирующей системе. Прежде всего при помощи изотопного метода было выяснено, что синтез белка начинается с N-конца и завершается C-концом, т.е. процесс протекает в направлении : NH2®COOH.
Белковый синтез, или процесс трансляции, может быть условно разделен на 2 этапа: активирование аминокислот и собственно процесс трансляции.
Второй этап матричного синтеза белка, собственно трансляцию, протекающей в рибосоме, условно делят на три стадии: инициации, элонгации и терминации.
Активирование аминокислот
Необходимым условием синтеза белка, который в конечном счете сводится к полимеризации аминокислот, является наличием в системе не свободных, а так называемых активированных аминокислот, располагающих своим внутренним запасом энергии. Активация свободных аминоксилот осуществляется при помощи специфических ферментов аминоацил –тРНК-синтетаз в присутствии АТФ. Этот процесс протекает в 2 стадии:
Обе стадии катализируются одним и тем же ферментом. На первой стадии аминокислота реагирует с АТФ и образуется пирофосфат и промежуточный продукт, который на второй стадии реагирует с соответствующей 3¢-ОН-тРНК, в результате чего образуется аминоацил –тРНК и освобождается АМФ. Аминоацил-тРНК располагает необходимым запасом энергии.
Аминокислота присоединяется к концевому 3¢-ОН-гидроксилу АМФ, который вместе с двумя остатками ЦМФ образует концевой триплет ЦЦА, являющийся одинаковым для всех транспортных РНК.
Процессы трансляции
Инициация
Инициация трансляции представляет собой событие, в ходе которого происходит образованиe комплекса, включающего Мет-тРНКiмет, мРНК и рибосому, где—тРНКiмет инициирующая метиониновая тРНКВ этом процессе участвуют не менее 10 факторов инициации, которые обозначают как elF (от англ. eukaryotic initiation factors) с указанием номера и буквы. Первоначально 40S субъединица рибосомы соединяется с фактором инициации, который препятствует её связыванию с 60S субъединицей, но стимулирует объединение с тройным комплексом, включающим Мет-тРНКiмет, eIF-2 и ГТФ. Затем этот теперь уже более сложный комплекс связывается с 5'-концом мРНК при участии нескольких elF. Один из факторов инициации (elF-4F) узнаёт и присоединяется к участку «кэп» на молекуле мРНК, поэтому он получил название кэпсвязывающего белка. Прикрепившись к мРНК, 40S субъединица начинает скользить по некодирующей части мРНК до тех пор, пока не достигнет инициирующего кодона AUG кодирующей нуклеотидной последовательности. Скольжение 40S субъединицы по мРНК сопровождается гидролизом АТФ, энергия которого затрачивается на преодоление участков спирализации в нетранслируемой части мРНК. В эукариотических клеках некодирующие участки мРНК имеют разную длину, но обычно от 40 до 80 нуклеотидов, хотя встречаются области с протяжённостью более 700 нуклеотидов.
Достигнув начала кодирующей последовательности мРНК, 40S субъединица останавливается и связывается с другими факторами инициации, ускоряющими присоединение 60S субъединицы и образование 80S рибосомы за счёт гидролиза ГТФ до ГДФ и неорганического фосфата. При этом формируются А- и Р-центры рибосомы, причём в Р-центре оказывается AUG-кодон мРНК с присоединённым к нему Мет-тРНКiмет.
В клетках есть 2 различающиеся по структуре тРНК, узнающие кодон AUG. Инициирующий кодон узнаёт тРНКiмет, а триплеты мРНК, кодирующие включение метионина во внутренние участки белка, прочитываются другой тРНКiмет
Элонгация
По завершении инициации рибосома располагается на мРНК таким образом, что в Р-центре находится инициирующий кодон AUG с присоединённой к нему Мет-тРНКiмет., а в А-центре — триплет, кодирующий включение первой аминокислоты синтезируемого белка. Далее начинается самый продолжительный этап белкового синтеза — элонгация, в ходе которого рибосома с помощью аа-тРНК последовательно «читает» мРНК в виде триплетов нуклеотидов, следующих за инициирующим кодоном в направлении от 5' к З'-концу, наращивая полипептидную цепочку за счёт последовательного присоединения аминокислот.
Включение каждой аминокислоты в белок происходит в 3 стадии, в ходе которых:
• аа-тРНК каждой входящей в белок аминокислоты связывается с А-центром рибосомы;
• пептид от пептидил-тРНК, находящейся в Р-центре, присоединяется к a-NH2-группe аминоацильного остатка аа-тРНК А-центра с образованием новой пептидной связи;
• удлинённая на один аминокислотный остаток пептидил-тРНК перемещается из А-центра в Р-центр в результате транслокации рибосомы.
Связывание аминоацил-тРНК в А-центре. Кодон мРНК, располагающийся в А-центре рядом с инициирующим кодоном, определяем природу аа¢-тРНКаа¢, которая будет включена в А-центр. аа¢-тРНКаа¢ взаимодействует с рибосомой в виде тройного комплекса, состоящего из фактора элонгации EF-1, аа¢-тРНКаа¢, и ГТФ Комплекс эффективно взаимодействует с рибосомой лишь в том случае, если антикодон аа¢-тРНКаа¢, комплиментарен и антипараллелен кодону мРНК в А-центре. Включение аа¢-тРНКаа¢, в рибосому происходит за счёт энергии гидролиза ГТФ до ГДФ и неорганического фосфата
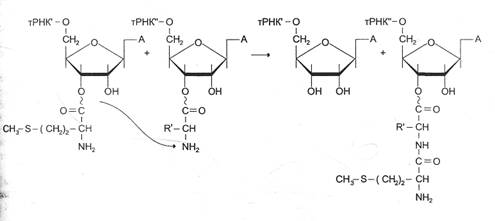
Образование пептидной связи происходит сразу же после отщепления комплекса EF-1 и ГДФ от рибосомы. Эта стадия процесса получила название реакции транспептидации.
В ходе этой реакции остаток метионина аа¢-тРНКаа¢, связывается с a-аминогруппой первой аминокислоты, присоединённой к тРНКаа¢, и pacположенной в А-центре, образуется первая пептидная связь. Установлено, что пептидилтранс|феразная активность большой субъединици рибосомы принадлежит 28S рРНК. К настоящему времени обнаружена целая группа РНК, обладающая свойствами ферментов. Эти каталитически активные РНК получили название рибозимов Полагают, что рибозимы можно считать «реликтами» раннего периода революции, когда белки ещё не приобрели такого значения, как в последующие периоды.
Транслокация — третья стадия элонгации. К рибосоме присоединяется фактор элонгации EF-2 и за счёт энергии ГТФ продвигает рибосому по мРНК на один кодон к З'-концу. В результате дипептидил-тРНК, которая не меняет своего положения относительно мРНК, из А-центра перемещается в Р-центр. Свободная от метионина тРНКаа¢, покидает рибосому, а в область А-центра попадает следующий кодон.
По завершении третьей стадии элонгации рибосома в Р-центре имеет дипептидил-тРНК, а в А-центр попадает триплет, кодирующий включение в полипептидную цепь второй аминокислоты. Начинается следующий цикл стадии элонгации, в ходе которого на рибосоме снова проходят вышеописанные события. Повторение таких циклов по числу смысловых кодонов мРНК завершает весь этап элонгации.
Терминация
Терминация трансляции наступает в том случае, когда в А-центр рибосомы попадает один из стоп-кодонов: UAG, UAA или UGA. Для стоп-кодонов нет соответствующих тРНК. Вместо этого к рибосоме присоединяются 2 белковых высвобождающих фактора RF (от англ, releasing/actor) или фактора терминации. Один из них с помощью пептидилтрансферазного центра катализирует гидролитическое отщепление синтезированного пептида от тРНК. Другой за счёт энергии гидролиза ГТФ вызывает диссоциацию рибосомы на субъединицы.
Интересно отметить, что факторы трансляции, реализующие эффекты за счёт гидролиза ГТФ, являются членами суперсемейства G-белков, в которое входят G-белки, участвующие в трансдукции сигналов гормонов и других биологически активных веществ, и Ras-белки, функционирующие как факторы роста. Все G-белки связывают и гидролизуют ГТФ. Когда они связаны с ГТФ, то активны и участвуют в соответствующих метаболических процессах, а когда в активном центре в результате гидролиза ГТФ превращается в ГДФ, эти белки приобретают неактивную конформацию.
Таким образом, матричная природа процесса трансляции проявляется в том, что последовательность поступления аминоацил-тРНК рибосому для синтеза белка строго детерминирована мРНК, т.е. порядок расположения кодонов вдоль цепи мРНК однозначно задает структуру синтезируемого белка. Рибосома сканирует цепь мРНК в виде триплетов и последовательно отбирает из окружающей среды «нужные» аа-тРНК, освобождая в ходе элонгаци деацилированные тРНК.
Малая и большая субъединицы рибосомы: процессе трансляции выполняют разные функции: малая субъединица присоединяет мРНК декодирует информацию с помощью тРНК механизма транслокации, а большая субъеданица ответственна за образование пептидных связей.
Полирибосомы
В процессе синтеза белка рибосома присоединяется к 5'-концу мРНК и перемещается в направлении З'-конца. При этом 5'-конец мРНК освобождается, и к нему может присоединиться новая рибосома, на которой начинается poст ещё одной полипептидной цепи. Как правило много рибосом одновременно участвует в синтезе белка на одной и той же мРНК, образуя комплекс, который называют полирибосомой, или полисомой.
Каждая рибосома занимает на мРНК участок длиной около 80 нуклеотидов, поэтому рибрсомы располагаются на мРНК с интервалом примерно в 100 нуклеотидов. Чем длиннее полипептидная цепочка синтезируемого белка, тем больше рибосом может одновременно осуществлять синтез этого белка, значительно увеличиваая таким образом эффективность использования матрицы.
Каждая рибосома способна катализировать образование около 100 пептидных связей в минуту. Полирибосомы могут существовать в виде частиц, плавающих в цитоплазме клеток, или могут быть связаны с ЭР. Свободные цитоплазматические полирибосомные частицы ответственны за синтез белков, выполняющих внутриклеточные функции. Полирибосомы, ассоциированные с ЭР, под электронным микроскопом имеют вид «шероховатой» поверхности. Белки, синтезируемые «шероховатым» ЭР, должны транспортироваться через мембрану для того, чтобы они достигли места окончательной локализации. Для них характерно присутствие на N-конце лидерной, или сигнальной, последовательности длиной от 15 до 30 аминокислотных остатков, которая содержит много аминокислот с гидрофобными радикалами и обеспечивает прохождение белка через липидный бислой мембран. Некоторые из этих белков для дальнейшего транспорта упаковываются аппаратом Гольджи в секреторные гранулы.
Дата: 2019-05-29, просмотров: 382.