Радиоактивность появились на земле со времени ее образования и человек за всю историю развития своей цивилизации находился под влиянием естественных источников радиации. Земля подвержена радиационному фону, источниками которого служат излучения Солнца, космическое излучение, излучение от залегающих в Земле радиоактивных элементов.
Термин радиоактивность, радиация по латыни звучит как излучение, с которым мы встречаемся каждый день, зажигая электрический свет (электромагнитное излучение), включая телевизор (излучение электронов) или загорая на солнце (ультрафиолетовое излучение). В дальнейшем под термином радиоактивность мы будем рассматривать ионизирующее излучение, т.е. излучение, действующее на вещество и изменяющее физическое состояние атомов в нем. Явление радиоактивности было открыто французским физиком А. Беккерелем 1 марта 1896 года при случайных обстоятельствах. Беккерель положил несколько фотографических пластинок в ящик своего стола и, чтобы на них не попал видимый свет, он придавил их куском соли урана. После проявления и исследования он заметил почернение пластинки, объяснив это излучением солью урана невидимых лучей. От солей урана Беккерель перешёл к чистому металлическому урану и отметил, что эффект испускания лучей усилился. Так произошло открытие радиоактивности.
Исследования показали, что эти лучи проникают сквозь тонкие металлические экраны и ионизируют газ, через который проходят. Их проникающая способность не зависит ни от температуры, ни от освещения, ни от давления. Их интенсивность не менялась со временем. Замечательной способностью обнаруженного излучения оказалась его самопроизвольность. Эти лучи, назвали позднее рентгеновскими.
Поисками веществ, способных к лучеиспусканию, по предложению Беккереля занялись молодой профессор Пьер Кюри и его супруга Мария Складовская-Кюри. Эти учёные обнаружили, что урановая смоляная руда обладает способностью давать излучение, в 4 раза превосходящее по интенсивности излучение урана. Это свидетельствовало о том, что в руде присутствовал источник излучения, более мощный, чем уран. В 1898 году супруги Кюри открыли два новых элемента — полоний, названный так в честь родины Марии Складовской-Кюри — Польши, и радий, что означает по латыни "испускающий лучи".
В честь супругов Кюри получил свое название искусственно полученный трансурановый элемент с номером 96 — Кюрий. Среди элементов содержащихся в земной коре, радиоактивными являются все начиная с висмута, т.е. с порядковым номером более 83 в таблице элементов Менделеева.
Вещества, испускающие новые излучения были названы радиоактивными, а новое свойство вещества, связанное с испусканием излучения, по предложению М. Кюри, было названо радиоактивностью.
Вскоре после открытия полония и радия Резерфордом было установлено, что радиоактивное излучение неоднородно по своему составу. Одна часть излучения поглощается тонкой алюминиевой фольгой, а другая проходила без изменения. Анализ состава излучения проводился по отклонению его в магнитном поле (рис. 1.1). Было обнаружено, что излучение содержит три вида лучей — альфа, бета, гамма.
Характер отклонения лучей в магнитном поле показывает, что альфа-лучи несут положительный заряд. Оказалось, что это атомы гелия, потерявшие два электрона, т.е. ядра атома гелия-4.
Ядро гелия-4 состоит из двух положительных протонов и двух нейтральных нейтронов. Все частицы в ядре связаны прочной связью и оно стабильно.
а-лучи — тяжелые частицы с малой проникающей способностью.
Бета-лучи — легкие частицы с большой проникающей способностью. Бета-лучи представляют собой поток быстро летящих электронов. Их скорость близка к скорости света.
у-лучи обладают максимальной проникающей способностью и представляют собою жесткое электромагнитное излучение. Гамма-лучи обладают относительно малой ионизирующей способностью, в тоже время они имеют большие частоты, чем рентгеновские лучи. Это свойство гамма-лучей привело к широкому использованию их в медицине, для лечения злокачественных опухолей, диагностике заболеваний и т.д.
СТРОЕНИЕ АТОМНОГО ЯДРА
Все тела независимо от их агрегатного состояния состоят из мельчайших "кирпичиков", которые назвали атомами. "Кирпичики" имеют различные типы связи в зависимости от того к какому химическому элементу таблицы Менделеева они принадлежат. Химический элемент — совокупность атомов одного типа. Древние греки считали атом неделимым, отсюда и произошел термин атом, "неделимый". Но, как показано выше, атом является источником радиоактивного излучения, поэтому рассмотрим его строение более подробно.
Английский учёный Джозеф Джон Томпсон, проводя исследование катодных лучей, возникающих при электрическом разряде в газах, впервые экспериментально обнаружил элементарные отрицательные заряды — электроны. Он же первый измерил удельный заряд электрона — е/т (отношение заряда электрона к его массе). Было установлено, что электроны вырываются из атомов. Атомы, представлявшиеся до этого неделимыми "кирпичиками мироздания", обнаружили тонкую структуру.
В 1903 г. после открытия электрона Томсон предложил модель атома в виде положительной объемно заряженной сферы диаметром 10~10 м, внутри которого, подобно изюму в кексе, вкраплены электроны. Отрицательный заряд электронов равен положительному заряду сферы. Излучение атомом Томсон объяснял колебаниями электронов относительно центра сферы. Из модели Томсона следовало, что масса атома распределялась равномерно по всему объему, однако, как позднее в 1908 году показал Э. Резерфорд в опытах по рассеянию «-частиц (ядер гелия тонкой золотой фольгой), это являлось ошибочным.
В качестве "зондирующих" частиц были выбраны альфа-частицы, преимущество которых перед другими видами излучений — в их высокой монохроматичности (все альфа-частицы, вылетающие из атомов одного сорта имеют одинаковую скорость) и в их большой массе (масса альфа-частицы превышает массу электрона в 7296 раз). Из-за своей большой массы альфа-частицы не должны испытывать соударений с электронами, содержащимися в атоме, и по их рассеиванию в веществе можно судить о распределении положительно заряженной материи в атоме.
Схема опытов Резерфорда представлена на рис. 1.2. Альфа-частицы испускались источником 1, помещенным внутри свинцовой камеры с узким каналом 2 так, чтобы все частицы, кроме движущихся вдоль оси канала, поглощались стенками камеры. Узкий пучок альфа-частиц попадал на тонкую золотую фольгу 3, перпендикулярно к её поверхности. Альфа-частицы, прошедшие через фольгу и рассеянные ею, попадали на экран и вызывали вспышки (сцинтилляции) на нем. В промежутке между фольгой и экраном создавался вакуум, чтобы не происходило дополнительного рассеяния альфа-частиц в воздухе.
Опыты показали, что в большинстве своем частицы после прохождения фольги сохраняли своё прежнее направление или отклонялись на очень малые углы. И лишь одна из 2 х 104 частиц отклонялась на угол, больший 90°. Для объяснения результатов этих опытов Резерфорд предположил, что весь положительный заряд сосредоточен в весьма малом объеме атома — ядре. Остальной объем атома заполнен электронами, полный отрицательный заряд которых равен положительному заряду ядра. Так в 1911 году была создана ядерная модель атома.
Рассеяние альфа-частиц в этой модели атома получило простое объяснение. В самом деле, так как электроны имеют весьма малую массу, по сравнению с альфа-частицей и распределены по всему объему атома, то а-частицы не должны испытывать заметного отклонения из-за взаимодействия с электронами. Только те частицы, которые проходят вблизи ядра испытывают сильное отклонение из-за кулоновских сил отталкивания между положительно заряженной частицей и массивным ядром. Но из-за малых размеров ядра вероятность встречи альфа-частицы с ядром также мала, поэтому и число альфа-частиц, испытавших отклонения на большие углы, весьма невелико.
На основании опытов Резерфорда по рассеянию альфа-частиц тонкими металлическими фольгами и теоретических расчетов была сформулирована ядерная модель ядра. По этой модели в центре атома — ядре, имеющем линейные размеры 10~ -10 м, сосредоточен весь положительный заряд атома и практически вся его масса. Вокруг атома, в области размером примерно 10 м, по орбитам движутся электроны, масса которых составляет весьма незначительную часть массы атома. Ядерная модель атомов напоминает солнечную систему: в центре системы находится "солнце" — ядро, а по орбитам вокруг него движутся "планеты" — электроны. "Планетарная" модель атома, дополненная постулатами Бора, оказалась весьма плодотворной для объяснения линейчатых спектров водородоподобных атомов, позволила объяснить природу характеристических рентгеновских спектров и ряд других физических явлений. В дальнейшем эта модель атома претерпела изменения, сохранив при этом свои основные черты. Атом состоит из ядра и электронов, расположенных вокруг ядра на определенных энергетических оболочках. Важнейшими характеристиками ядра являются его заряд Z и масса М.
В 1911 г. в опытах Резерфорда по облучению альфа-частицами легких газов показано, что ядра расщепляются, с вылетом ядер водорода, которые впоследствии были названы протонами. Эти эксперименты показали, что протоны являются составной частью ядра.
В 1932 г. английский физик Дж. Чедвиг провел опыты по бомбардировке бериллиевой фольги альфа-частицами и открыл еще одну ядерную частицу — нейтрон, который по своей массе был близок к протону.
Заряд ядра определяется числом элементарных положительных зарядов, содержащихся в нем, и совпадает с порядковым номером химического элемента в таблице Менделеева. Носителем элементарного положительного заряда является протон. Заряд протона (р) q = +1,6021 х Ю~19 Кл, масса покоя протона М = 1,6726 хЮ"26 кг =1836Ме (Ме = 9,11хЮ~31 кг). В состав ядра, кроме протонов, входят нейтроны. Нейтрон (п) — нейтральная частица с массой покоя Мп = 1,6749 х 10~27 кг = 1839Ме.
В ядерной физике считается, что протон и нейтрон — два так называемых зарядовых состояния одной и той же частицы — нуклона (от латинского nucleus — ядро). Протон является протонным состоянием нуклона с зарядом +е , нейтрон — его нейтронным состоянием с нулевым зарядом. Нуклоны в ядре находятся в состояниях, отличных от их свободных состояний. Это связано с тем, что в ядре между нуклонами осуществляется особое ядерное взаимодействие. От электромагнитного взаимодействия оно отличается тем, что одинаково действует на заряженный протон и нейтральный в элементарном отношении нейтрон. Действие ядерного взаимодействия проявляется на очень близких ядерных расстояниях (около 10~13 м), величина очень велика, позволяющая сжать ядерное вещество до плотности сотни миллионов тонн в 1 см3.
Масса атомного ядра совпадает практически с массой всего атома, т.к. масса электронов мала. Ядро, как и нейтральный атом, символически обозначаются так АгХ , где X — символ химического элемента, Z — атомный номер (число протонов в ядре), А — массовое число (число нуклонов в ядре). Массы атомов принято выражать в атомных единицах массы (а. е. м.). За атомную единицу массы принята 1/16 массы атома кислорода:
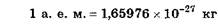
Кроме того применяется "унифицированная атомная единица массы" (у. а. е. м.), равная 1/12 массы атома углерода:
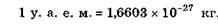
В природе существуют множество радиоактивных веществ, в соответствии со своими свойствами они объединены в ряды тория и урана. Однако и среди них встречаются вещества с одинаковыми химическими свойствами но с различными массами. Эти вещества были названы изотопами (от греческих слов "одинаковый" и "место"), т.е. ядра с одинаковыми Z , но разными А (т.е. с разными числами нейтронов N = А - Z). Например, водород ( Z = 1) имеет три изотопа: 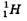 — протий ( Z = 1, N = 0),
— протий ( Z = 1, N = 0), 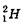 — дейтерий ( Z = 1, N = 1),
— дейтерий ( Z = 1, N = 1), 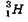 — тритий ( Z = 1, N = 2). Ядра с одинаковыми А, но разными Z называются изобарами. Примером ядер-изобар могут служить
— тритий ( Z = 1, N = 2). Ядра с одинаковыми А, но разными Z называются изобарами. Примером ядер-изобар могут служить 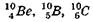 .
.
РАДИОАКТИВНЫЙ РАСПАД
В 1911 году Резерфорд и Содди показали, что атомы некоторых веществ испытывают последовательные превращения, образуя радиоактивные ряды, где каждый член этого ряда возникает из предыдущего, причем никакими внешними физическими воздействиями (температура, электрические и магнитные поля, давление) нельзя повлиять на характеристики распада.
Позже, способность некоторых ядер самопроизвольно (спонтанно) превращаться в другие ядра с испусканием различных видов излучения и элементарных частиц называли радиоактивностью. При этом различают два вида радиоактивности — естественную, наблюдающуюся у нестабильных изотопов атома, существующих в природе, и искусственную, наблюдающуюся у изотопов, образующихся в результате ядерных реакций. Оба вида радиоактивности ничем принципиально не отличаются друг от друга и описываются одними и теми же законами радиоактивных превращений.
Процесс естественного, самопроизвольно происходящего радиоактивного превращения называется радиоактивным распадом, или просто распадом. Ядра, испытывающие распад, называются радионуклидами. Исходное атомное ядро называется материнским, а ядро, образовавшееся в результате распада, называется дочерним.
Радиоактивный распад происходит со строго определённой скоростью, характерной для каждого данного элемента. Время, за которое исходное число радиоактивных ядер в среднем уменьшается вдвое, называется периодом полураспада Т. Периоды полураспада различных ядер колеблются в очень широких пределах. Так, например, период полураспада урана 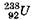 составляет 4,5 млрд. лет, радия
составляет 4,5 млрд. лет, радия 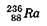 — 1620 лет, радона—
— 1620 лет, радона— 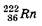 3,8 суток. Более того, периоды полураспада у изотопов одного и того элемента могут сильно различаться — у
3,8 суток. Более того, периоды полураспада у изотопов одного и того элемента могут сильно различаться — у 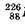 Ra Т = 1630 лет, а у
Ra Т = 1630 лет, а у 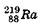 Т=0,001с.
Т=0,001с.
Поскольку отдельные радиоактивные ядра распадаются независимо друг от друга, то закон радиоактивного распада носит статистический характер. Можно показать, что закон убывания во времени числа радиоактивных ядер данного вещества (закон радиоактивного распада) имеет вид 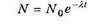
Здесь 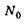 — число радиоактивных ядер в момент времени, принятый за начало отсчёта, т.е. при t = 0 . N — число радиоактивных ядер в момент времени t . Я — постоянная для данного радиоактивного вещества величина, носящая название постоянной радиоактивного распада. Между постоянной радиоактивного распада и периодом полураспада существует простая связь:
— число радиоактивных ядер в момент времени, принятый за начало отсчёта, т.е. при t = 0 . N — число радиоактивных ядер в момент времени t . Я — постоянная для данного радиоактивного вещества величина, носящая название постоянной радиоактивного распада. Между постоянной радиоактивного распада и периодом полураспада существует простая связь:
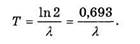
Среднее время жизни радиоактивного ядра г есть величина, обратная постоянной радиоактивного распада, т.е. радионуклиды, из которых 37000 распадается каждую 5 секунду.
Радиоактивный распад происходит в соответствии с правилами смещения, установленными опытным путём. Правила смещения: => для альфа-распада (превращения ядер, сопровождающиеся испусканием альфа-частиц)
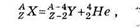 :=>
:=>
для бета распада (превращения ядер, сопровождающиеся, испусканием бета-частиц)
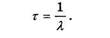
Активностью А нуклида в радиоактивном источнике называется число распадов, происходящих с ядрами образца в единицу времени:
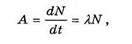
где 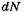 — число ядер, распавшихся в среднем за интервал времени от t до t + dt .
— число ядер, распавшихся в среднем за интервал времени от t до t + dt .
Единица активности в системе СИ — беккерелъ (Бк): 1 Бк — активность нуклида, при которой за 1 с происходит один распад. Внесистемная единица активности — кюри (Ки):
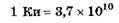 Бк.
Бк.
1 кюри равен числу распавшихся ядер содержащихся в 1 г радия за 1 с (3,7 х 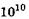 рас/сек).
рас/сек).
Милликюри — 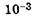 Ки.
Ки.
Микрокюри — 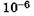 Ки.
Ки.
На всех картах радиационного загрязнения, явившегося результатом Чернобыльской катастрофы, приводится радиационная плотность загрязнения, т.е. радиоактивность на единицу площади.
Например, если вы проживаете на территории с плотностью загрязнения почвы 1 Ки/кв. км или 37000 Бк/кв. м (37 кБк/кв. м), то это означает, что на одном квадратном метре этой почвы находятся
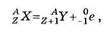
где X — химический символ материнского ядра, 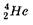 — ядро атома гелия,
— ядро атома гелия, 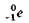 — символическое обозначение электрона (заряд его равен —1, массовое число равно 0).
— символическое обозначение электрона (заряд его равен —1, массовое число равно 0).
Правила смещения являются следствиями двух законов сохранения, выполняющихся при радиоактивных распадах — сохранения электрического заряда и массового числа: сумма зарядов (массовых чисел) возникающих ядер и частиц равна заряду (массовому числу) исходного ядра.
Получившееся в результате распада дочернее ядро тоже может быть радиоактивным. В результате возникает цепочка или ряд радиоактивных превращений, заканчивающихся стабильным изотопом. Совокупность элементов, образующих цепочку, называется радиоактивным семейством. Семейство называется по наиболее долгоживущему элементу (с наибольшим периодом полураспада) "родоначальнику" семейства: тория 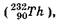 урана
урана 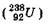 и актиния. Конечными
и актиния. Конечными 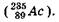 нуклидами являются соответственно
нуклидами являются соответственно
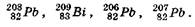
В таблице 1 представлена цепочка семейства урана.
 Таблица 1. Семейство урана.
Таблица 1. Семейство урана.
| Вид излучения | Нуклид | Период полураспада |
| α | Уран-238 | 4,47 млрд.лет |
| β | Торий-234 | 24,1 суток |
| β | Протактиний-234 | 1,17 минут |
| α | Уран-234 | 245000 лет |
| α | Торий-230 | 8000 лет |
| α | Радий-226 | 1600 лет |
| α | Радон-222 | 3,823 суток |
| α | Полоний-218 | 3,05 минут |
| β | Свинец-214 | 26,8 минут |
| β | Висмут-214 | 19,7 минут |
| α | Полоний-214 | 0,000164 секунды |
| β | Свинец-210 | 22,3 лет |
| β | Висмут-210 | 5,01 суток |
| β | Полоний-210 | 138,4 суток |
| Свинец-206 | стабильный |
Дата: 2019-05-29, просмотров: 328.