В настоящее время известно значительное число методов получения как частично симметричных, так и полностью несимметричных порфиринов через b-билены.
Этот метод достаточно широко используется для синтеза сложных порфиринов, этому способствует ряд обстоятельств: а) более легкий синтез исходных дипирролилметанов по сравнению с получением аналогичных 5,5’-диалкоксикарбонильных соединений, которые необходимы в методе Макдональда; б) отсутствие гексапирродиенов при синтезе биленов; в) возможность получения полностью несимметричных порфиринов. Следует отметить, что при синтезе диацетилпорфирина было показано, что при получении порфиринов с одной и особенно с двумя электроотрицательными группами синтез биленов надо планировать таким образом, чтобы эти заместители находились в крайних пиррольных кольцах. При наличии подобных заместителей в дипирролилметановом фрагменте билена повышалась чувствительность метинового мостика к электрофильным реакциям. Возможность побочных реакций особенно возрастала, когда два таких заместителя расположены в противоположных пиррольных кольцах. С учетом сказанного был синтезирован замещенный цитопорфирин (40), который является ключевым соединением при получении порфирина α, выход составил 30%.
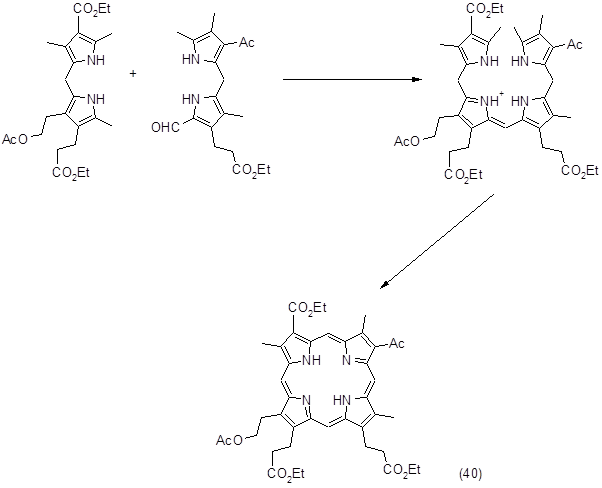
В заключение можно отметить, что использование b‑биленов в качестве промежуточных соединений позволяет получать широкий круг порфиринов с различными заместителями. Среди недостатков этого метода следует отметить недостаточную устойчивость b-биленов и их подверженность нежелательным превращениям.
Циклизация а,с-биладиенов.
Биладиены, среди прочих тетрапиррольных структур, играют важную роль в природе (желчные пигменты и протеины) и являются интермедиатами в синтетических подходах к природным порфиринам [65]. В 1966 году Джонсон предложил оригинальный метод синтеза порфиринов, который позволяет получать как симметричные, так и несимметричные порфирины [66].
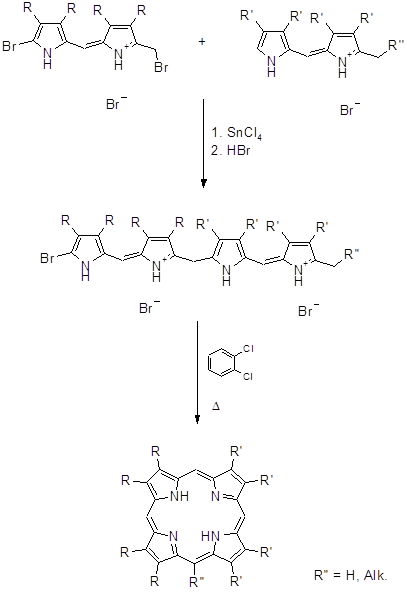
Данный способ нашел применение для алкилзамещенных порфиринов. Выход выше изображенного порфирина на последней стадии составил ~ 70%. На основе а,с- биладиенов также были синтезированы производные мезо-аминопорфирина при аномальной циклизации 1,19-диметил-а,с-диметил-а,с-биладиенов с Cu(OAc)2 в ДМФА, причем мезо-углеродный атом порфиринового макроцикла образуется из карбонильного углерода ДМФА [8,67,68].
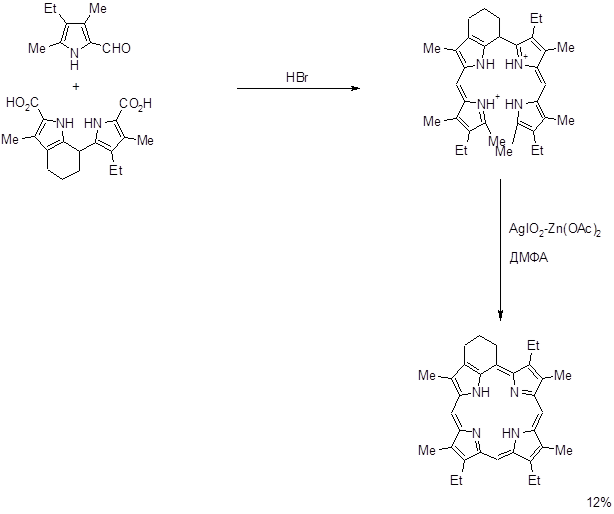
2.2.3. “3+1” порфириновый синтез.
Этот способ позволяет получать как симметричные, так и несимметричные порфирины и их аналоги, причем, выход может достигать отличных для порфиринового синтеза значений ‑ 40-50% [69]. Метод состоит в конденсации трипирана с 2,5‑диформилпирролом [70] или 2,5-бис[(N,N-диметиламино)метил]пирролом [52,71]. Синтез с 2,5‑диформилпирролом используется наиболее часто, его проводят, когда исходные субстраты способны выдержать условия кислотного катализа, либо при однозначном образовании одного изомера порфирина или возможности легкого разделения смеси изомеров. Недостатком выше описанного метода, являлась сложность синтеза 2,5‑диформилпирролов, однако в последние годы был разработан достаточно простой и надежный способ позволяющий получать пиррол дикарбальдегиды с хорошим выходом [6,70,72,73].
Другим возможным вариантом «3+1» порфиринового синтеза является использование 2,5‑бис[(N,N‑диметиламино)метил]пиррола, при этом реакция проводится в более мягких условиях, за счет чего достигается образование одного изомера порфирина, а не всех возможных как при использовании 2,5‑диформилпирролов [52]. При помощи этого метода стало возможным синтезировать азапорфирины, содержащие в качестве одного из пиррольных циклов имидазольный фрагмент, с удовлетворительным выходом [71].

Обсуждение результатов.
Порфириновые макроциклы сопряженные по b-положениям пиррольного кольца с ароматическими и гетероциклическими системами нашли применение в качестве молекулярных зондов, высокоэффективных катализаторов, фотосенсоров в фотодинамической терапии рака и красителей поглощающих в ближнем ИК диапазоне спектра. Целью данной работы является поиск подходов к синтезу сопряженной системы пиррола с гетероциклическим фрагментом для последующего введения ее в порфириновый цикл.
Из литературных источников известно, что существует несколько подходов к синтезу порфиринового макроцикла, наиболее часто используемыми являются методы “2+2” и “3+1. Последний метод был выбран как наиболее подходящий. Для его реализации необходимо было синтезировать b-алкил или b-незамещенный трипиран и пиррол, содержащий в b-положениях функциональные заместители. С этой целью был синтезирован трипиран по следующей схеме:
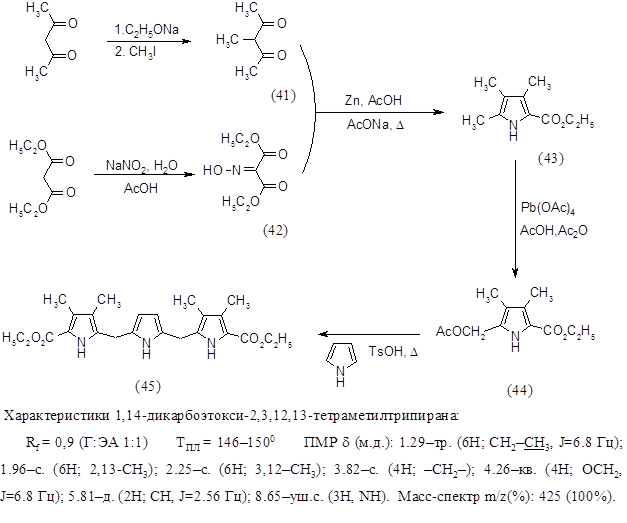
Алкилирование ацетилацетона проводили по стандартной методике - с применением на первой стадии этилата натрия и последующей обработкой метилиодидом при 400 в течение 1 часа, выход 3–метил–2,4–пентандиона (41) составил 48%. Синтез 2‑карбоэтокси-3,4,5‑триметилпиррола (43) проводили из 3-метил-2,4-пентандиона (41) и изонитрозомалонового эфира (42) конденсацией в уксусной кислоте в присутствии цинка и ацетата натрия при нагревании до 900 в течение 1 часа, выход продукта составил 71%. 2‑ацетоксиметил–3,4–диметил–5–карбоэтоксипиррол (44) получали окислением 2‑карбоэтокси-3,4,5-триметилпиррола (43) тетраацетатом свинца в смеси уксусной кислоты и уксусного ангидрида при комнатной температуре в течение 2 часов, выход 2‑ацетоксиметил–3,4–диметил–5–карбоэтоксипиррола (44) составил 82%. Синтез 1,14-дикарбоэтокси-2,3,12,13-тетраметил трипирана (45) проводили конденсацией в метаноле 1 эквивалента пиррола и 2 эквивалентов 2‑ацетоксиметил–3,4–диметил–5–карбоэтоксипиррола (44) в присутствии толуолсульфокислоты при нагревании до 600 в течение 7 часов, выход 1,14-дикарбоэтокси-2,3,12,13-тетраметил трипирана (45) составил 51%. Все синтезированные продукты были охарактеризованы спектральными методами и были определены их физико-химические константы.
Следующим этапом работы была разработка методов получения монопиррольных интермедиатов для получения сопряженной системы, включающей два гетероциклических фрагмента. Из литературных данных известно, что существует 2 подхода к синтезу сопряженной системы пиррола с гетероциклическим фрагментом:
1. К готовому гетероциклическому фрагменту, используя реакцию Бартона-Зарда, присоединяют пиррольный цикл.
2. К готовому пиррольному циклу, имеющему функциональные группы в b-положениях наращивают гетероциклический фрагмент.
На основе первого подхода было решено провести конденсацию 2-метил-6-нитробензотиазола (47) и этилового эфира изоциануксусной кислоты (51) в присутствии сильных ненуклеофильных оснований, т.е. в условиях реакции Бартона-Зарда [7,20,21].
Нитрование 2-метилбензотиазола (46) проводили нитрующей смесью при нагревании до 900 в течение 5 часов, выход 2-метил-6-нитробензотиазола (47) составил 20%.
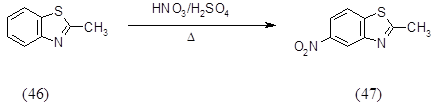
Исходным соединением в синтезе этилового эфира изоциануксусной кислоты (51) являлся глицин (48), который превращали в хлоргидрат глицинэтилового эфира (49) действием тионилхлорида в этаноле при кипячении с обратным холодильником в течение 2 часов. Выход продукта составил 94%. Полученный хлоргидрат глицинэтилового эфира (49) кипятили в этилортоформиате в присутствии толуолсульфокислоты и триэтиламина в течение 20 часов. Получили этиловый эфир N-формилглицина (50) с выходом 66%, который после обработки POCl3 в триэтиламине и дал этиловый эфир изоциануксусной кислоты (51) с выходом 76%. Все синтезированные продукты были охарактеризованы спектральными методами и были определены их физико-химические константы [16].
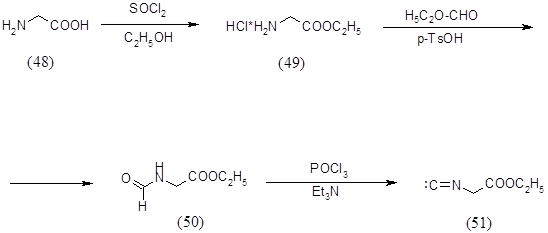
Полученные 2-метил-6-нитробензотиазол (47) и этиловый эфир изоциануксусной кислоты (51) растворяли в абсолютном ТГФ и вводили в конденсацию в присутствии сильных оснований (условия проведения реакций и обработка приведены в таблице). Однако реакция протекала плохо, в основном возвращался исходный 2-метил-6-нитробензотиазол (47) и получалось множество продуктов, суммарный вес которых незначителен.
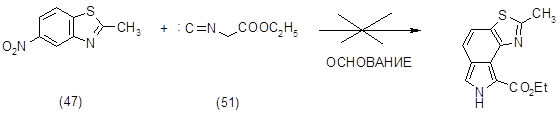
Реакция 2-метил-6-нитробензотиазола и этилового эфира изоциануксусной кислоты.
| Отношение 2‑метил‑6‑нитробензотиазола к этиловому эфиру изоциануксусной кислоты. | Растворитель, объем (на 0,1 г 2-метил-6-нитробензотиазола) (мл) | Основание, отношение к 2‑метил‑6‑нитробензотиазолу | Условия проведения реакции, обработка. |
| 1:1.1 | ТГФ абс. , 50 мл | DBU, 1: 1.1 | 100 часов при комнатной температуре. |
| 1:1.1 | ТГФ абс. , 50 мл | DBU, 1: 1.1 | Кипячение 12 часов. |
| 1:1.1 | ТГФ абс. , 50 мл | (Et2N)3P=NEt, 1:1 | 24 часа при 200 и 4 часа при 600, разбавляют CHCl3 и промывают водой. |
| 1:1.1 | ТГФ абс. , 50 мл | (Et2N)3P=NEt, 1:2 | 200 часов при 200, разбавляют CHCl3 и промывают водой. |
| 1:1.1 | ТГФ абс. , 50 мл | (Et2N)3P=NEt, 1:2 | 200 часов при 500, разбавляют CHCl3 и промывают водой. |
| 1:1.1 | ТГФ абс. , 40 мл | NaH, 1:1 | 72 часа при при 200, разбавляют CHCl3 и промывают водой. |
| 1:1.1 | ТГФ абс. , 40 мл | NaH, 1:2 | 72 часа при при 200, разбавляют CHCl3 и промывают водой. |
| 1:1.1 | ТГФ абс. , 40 мл | NaH, 1:2 | 72 часа при при 500, разбавляют CHCl3 и промывают водой. |
Использование данного подхода было признано не эффективным, таким образом, было решено перейти к второму подходу. Предполагалось присоединить тиазольный или имидазольный фрагмент по b-положениям пиррола. С этой целью необходимо было разработать удобные методы синтеза b,b’-диаминопиррола или b-галоген-b’-аминопиррола. Аминогруппы предполагалось получать путем восстановления нитрогрупп, и задача сводилась к получению нитропирролов.
Первоначально для нитрования был выбран 2,5-диметилпиррол (56), который был синтезирован по следующей схеме:
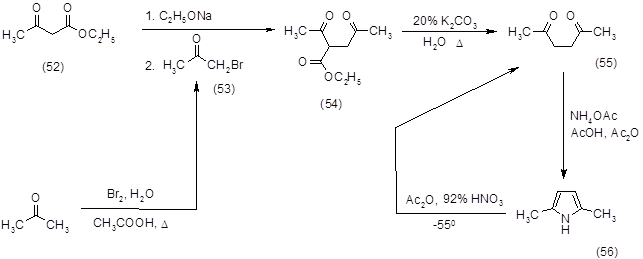
Алкилирование ацетоуксусного эфира (52) проводили бромацетоном (53), полученным предварительно с выходом 40% при обработке ацетона бромом в водной уксусной кислоте при 700 в течение 2 часов. Алкилирование ацетоуксусного эфира (52) проводили двумя способами: 1) с использованием катализатора межфазного переноса [74]; 2) по стандартной методике с использованием этилата натрия. Выход реакции алкилирования по первому методу составил 20%, а по второму – 53%, поэтому для наработки ацетонилацетоуксусного эфира (54) был выбран последний способ. Полученный ацетонилацетоуксусный эфир (54) декарбоксилировали при кипячении с обратным холодильником в течение 1 часа 20% водным раствором поташа. Выход 2,5-гександиона (55) составил 65%. Замыкание полученного 2,5-гександиона (55) в пиррольный цикл проводили ацетатом аммония в смеси уксусной кислоты и уксусного ангидрида при комнатной температуре в течение 0,5 часа. Выход 2,5-диметилпиррола (56) составил 57%. Нитрование 2,5-диметилпиррола (56) проводили при –550 смесью 92% HNO3 и уксусного ангидрида, однако, даже в таких мягких условиях произошло раскрытие цикла, и в качестве продукта был выделен 2,5-гександион (55). Все синтезированные продукты были охарактеризованы спектральными методами и были определены их физико-химические константы.
Так как известно, что введение акцепторных заместителей приводит к стабилизации пиррольного цикла, поэтому было решено вводить нитрогруппы в пиррол, содержащий акцепторные группы. С этой целью в качестве соединения для введения нитрогрупп был выбран 2,5-диформилпиррол (61).
Существующие методики получения 2,5-диформилпирролов [75-82] отличаются многостадийностью, малой доступностью исходных реагентов и умеренными выходами. Поэтому необходимо было разработать простой и эффективный метод получения этого соединения.
В качестве исходного соединения был выбран пиррол. Введение первой формильной группы не представляет труда и описано в литературе [83]. Формилирование пиррола (57) проводили по стандартной методике комплексом Вильсмеера при 350 в течение 0,5 часа, гидролиз проводили при кипячении в водном растворе ацетата натрия в течение 0,5 часа, выход 2-формилпиррола (58) составил 64%. Прямое формилирование 2-формилпиррола (58) приводит главным образом к 2,4-диформилпирролу и к 0,3% 2,5-диформилпиррола (61) [75]. Для введения альдегидной группы в 5-положение необходимо было ввести группу с одной стороны направляющую в это положение, а с другой стороны легко снимаемую в результате обработки. В качестве такой группы была выбрана дикарбоэтоксивинильная группа. 2-(Пиррол-2-илметилен)малоноат (59) получали при кипячении в бензоле 2-формилпиррола (58) и диэтилмалонового эфира в присутствии пиперидина и уксусной кислоты в течение 1 часа. Продукт без дополнительной очистки был направлен на следующую стадию.

Формилирование 2-(пиррол-2-илметилен)малоноата (59) проводили комплексом Вильсмеера при 400. В зависимости от условий проведения гидролиза полученной соли возможно выделить продукт формилирования без снятия защитной группы. Так при проведении гидролиза насыщенным раствором ацетата натрия при комнатной температуре образуется 2‑[(5‑формилпиррол-2-ил)метилен]малоноат (60) с выходом 55%, который был полностью охарактеризован спектральными методами и физико-химическими методами и имеет следующие характеристики: Rf = 0,7 (Хл:МеОН 9:1); ТПЛ = 98–1000; ПМР d (м.д.): 1.31–тр. (3H; CH2CH3, J=7.26 Гц); 1.37–тр. (3H; CH2CH3, J=7.26 Гц); 4.30–кв. (2H; CH2, J=7.26 Гц); 4.38–кв. (2H; CH2, J=7.26 Гц); 6.68–д.д. (1H; CH, J=2.14 Гц); 6.94–д.д. (1H; CH, J=2.14 Гц); 7.57–c. (-CH=C); 9.65‑с. (CHO); 11.53‑уш.c. (1H; NH); 13С‑ЯМР d (м.д.): 13.88 (OCH2CH3); 13.99 (OCH2CH3’); 61.60 (О‑CH2); 62.11 (О‑CH2’); 119.53 (=С-); 120.49 (С‑4); 121.92 (С-3); 131.85 (C-5); 134.09 (-C=); 135.63 (C-2); 163.30 (С=О); 166.66 (С=О’); 179.78 (CHO). ИК (вазелиновое масло) n (cм‑1): 3300, 1730, 1700, 1670, 1620, 1550. Масс-спектр m/z (%): 265 (71%), 173 (100%), 145 (46%), 119 (30%), 91 (28%), 65 (30%), 39(15%).
При гидролизе с применением 3М NaOH и кипячении в течение 1 часа образуется 2,5-диформилпиррол (61) с выходом 53%, который был охарактеризован спектральными методами и физико-химическими методами и имеет следующие характеристики: Rf = 0,3 (Хл:МеОН 9:1); ТПЛ = 112–1140; ПМР d (м.д.): 7.02–д. (2H; CH, J=2 Гц); 9.77‑с. (2H; CHO); 10.38‑уш.c. (1H; NH); ИК (вазелиновое масло) n (cм‑1): 3140, 1720, 1700. Масс-спектр m/z (%): 123 (65%), 94 (18%), 66 (60%), 39(100%).
Полученный 2,5-диформилпиррол (61) предполагалось пронитровать в b-положение. В качестве нитрующего агента использовали смесь 98% HNO3 и уксусного ангидрида. По литературным данным известно, что пиррольный цикл, содержащий акцепторные группы должен быть устойчив в указанных условиях. Действительно разрушения цикла не происходило, однако одна из альдегидных групп окислилась, о чем свидетельствует спектр ПМР выделенного продукта (62): ПМР (CDCl3-CD3OD) d (м.д.): 6.15–д. (1H; CH, J=4 Гц); 6.68–д. (1H; CH, J=4 Гц); 7.94‑с. (1H; CHO).
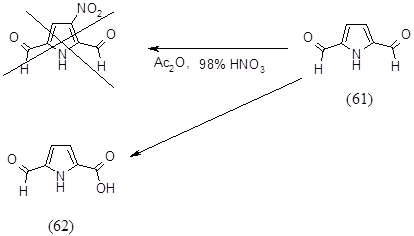
Поэтому было решено проводить реакцию нитрования 2,5-диметил-3-карбоэтоксипиррола (63). Данный пиррол был получен конденсацией ацетонилацетоуксусного эфира (54) ацетатом аммония в смеси уксусной кислоты и уксусного ангидрида при комнатной температуре в течение 20 минут с выходом 76%, характеристики полученного продукта совпали с литературными данными [84].
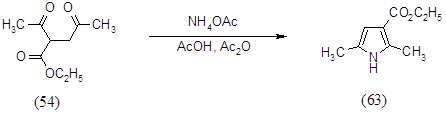
На этот раз прямое нитрование решили не использовать, так как велика вероятность раскрытия цикла и нитрогруппу решили вводить реакцией замещения галогена в b-положении на нитрогруппу при помощи нитрита серебра. Реакцию проводили двумя способами:
1) одностадийный метод с использованием нитрита серебра и йода в ацетонитриле;
2) двух стадийный метод, включающий первоначальное введение галогена, который затем замещается на нитрогруппу.
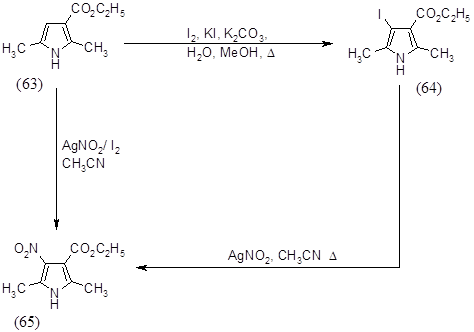
По первому способу введение нитрогруппы проводили обработкой 2,5-диметил-3-карбоэтоксипиррола (63) в ацетонитриле смесью нитрита серебра и йода в соотношении 2:1 при комнатной температуре в инертной атмосфере в течение 48 часов, выход 2,5-диметил-3-карбоэтокси-4-нитропиррола (65) составил 18%, соединение было полностью охарактеризовано спектральными методами и физико-химическими методами и имеет следующие характеристики: Rf=0.5(ПЭ:ЭА 1:1); Тпл= 110-1120 ; ПМР(CDCl3) d (м.д.): 1.35 м.д.-тр.(3Н, СН2‑СН3, J=7.1Гц); 2.35 м.д.-с.(3Н, СН3 ); 2.48 м.д.-с.(3Н, СН3); 4.32 м.д.-кв.(2Н, СН2-СН3, J=7.1Гц); 8.91 м.д.-уш.с.(1Н, NH). ИК(вазелиновое масло) n (см–1) : 3300, 1720, 1680, 1600. Масс-спектр m/z(%): 212 (19%), 166 (40%), 122 (43%), 92 (45%), 66 (28%), 54 (19%), 42 (100%).
По второму способу сначала необходимо было получить b-галогензамещенный пиррол. Иодирование 2,5-диметил-3-карбоэтоксипиррола (63) проводили в водно-метанольной смеси йодом в присутствии KI и поташа при 650 в течение 1,5 часов, выход 2,5-диметил-3-йод-4-карбоэтоксипиррола (64) составил 80%, соединение было полностью охарактеризовано спектральными методами и физико-химическими методами и имеет следующие характеристики: Rf = 0,7 (Г:ЭА 1:1); ТПЛ =116-1200; ПМР (CDCl3) d (м.д.):1.34-тр. (3H; -CH2CH3; J=7.24 Гц) 2.22–с. (3H; CH3); 2.47–c. (3H; CH3); 4.26–кв. (2H; CH2; J=7.24 ГцРРHHsss); 8.18‑уш.c. (1H; NH). 13С‑ЯМР (CDCl3) d (м.д.): 13.89 (2-CH3); 14.19 (3-CH3); 14.30 (OCH2CH3); 59.58 (C-I); 63.03 (‑CH2-); 129.48 (C-5); 129.55 (C-4); 135.58 (C-2); 164.62 (C=O). ИК(вазелиновое масло) n (см‑1): 3256, 1675, 1217, 1099, 1029, 773. Масс спектр m/z (%): 293 (40%), 279 (20%), 264 (42%), 248 (28%), 219 (8%), 127 (12%),122 (25%), 93 (30%), 67 (35%), 51 (55%), 42 (100%).
Реакцию замещения йода на нитрогруппу проводили при кипячении 2,5-диметил-3-йод-4-карбоэтоксипиррола (64) с нитритом серебра в ацетонитриле в течение 2 часов, выход 2,5-диметил-3-карбоэтокси-4-нитропиррола (65) составил 47%. Таким образом, второй метод оказался более предпочтительным, так как суммарный выход по этому способу составляет 37%, а по первому методу - 18%.
Также предполагалось омылить и декарбоксилировать полученный 2,5-диметил-3-йод-4-карбоэтоксипиррол (64) для дальнейшего введения нитрогруппы, однако омыление в различных условиях приводило лишь к отщеплению йода (условия проведения реакций и обработка приведены в таблице).
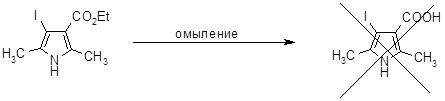
Омыление 2,5-диметил-3-иод-4-карбоэтоксипиррола.
| Омыляющий реагент. | V, (мл) | Растворитель | V (на 0,5 г пиррола, мл) | Условия реакции, обработка. | Время реакции. | Продукт реакции омыления. | ||
| H3PO4 | 2 мл | – | – | 1200 | 30 мин. | Выделяется I2, пиррол осмоляется. | ||
| 20% раствор NaOH | 2.16 мл | MeOH | 4 мл | Кипячение, подкисляют конц. HCl | 5,5 ч. | – “ – “ – | ||
| 20% раствор NaOH | 2.16 мл | MeOH | 4 мл | Кипячение, подкисляют H3PO4: H2O 1:5 | 4 ч. | – “ – “ – | ||
| H2SO4 конц. | 1.5 мл | – | – | 400, промывают водой | 30 мин. | – “ – “ – | ||
| 30% раствор NaOH | 2.16 мл | MeOH | 5 мл | Кипячение, подкисляют конц. HCl | 2 ч. | – “ – “ – | ||
| H2SO4 конц. | 1.5 мл | – | – | 200, промывают водой | 2 ч. | – “ – “ – | ||
Для синтеза нитро-галогензамещенного пиррола было решено использовать метод, описанный выше, поэтому необходимо было синтезировать b,b’-дийодпиррол.
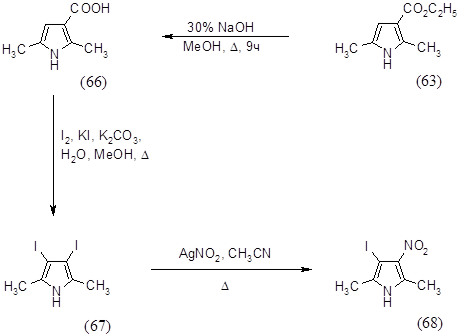
Указанное соединение получали в две стадии: первоначально проводили омыление 2,5-диметил-3-карбоэтоксипиррола (63) кипячением с 30% NaOH в метаноле в течение 9 часов, выход 2,5-диметил-3-карбоксипиррола (66) составил 65%; иодирование проводили в водно-метанольной смеси йодом в присутствии KI и поташа при 650 в течение 1,5 часов, выход 2,5-диметил-3,4-дийодпиррола (67) составил 45%. Соединение было охарактеризовано спектральными методами и физико-химическими методами и имеет следующие характеристики: Rf = 0,8 (Г:ЭА 1:3); ТПЛ =116-1200 (разл.); ПМР d (м.д.): 2.28–с. (6H; CH3); 8.01‑уш.c. (1H; NH); Масс спектр m/z (%): 347 (100%).
Реакцию замещения йода на нитрогруппу проводили по отработанной методике - при обработке 2,5-диметил-3,4-дийодпиррола (67) с нитритом серебра в ацетонитриле в течение 24 часов при комнатной температуре. В результате хроматографирования на колонке с силикагелем, было выделено 3 продукта (А, Б, В), которые были проанализированы с помощью Н1‑ЯМР спектроскопии. ПМР (CD3OD) d (м.д.): (А)‑ 2.21-с.(1Н); 2.54-c. (1H). (Б)- 1.45-c.(4H); 1.47-c.(18H); 2.18-c.(6H); 2.41-c.(4H); 3.35-c.(4H). (B)-1.43-c.(9H); 1.46-д.(2H); 1.62-c.(1H); 1.87‑c.(1H); 1.98-д.(2H); 2.42-c.(3H); 3.34-c.(3H); 6.51-c.(3H).
Основным является продукт (А) в ПМР-спектре которого наблюдалось 2 синглета одинаковой интенсивности в области 2.21 и 2.54 м.д., что позволило предположить о наличие двух неэквивалентных метильных группы в пиррольном кольце. Полученное соединение было проанализировано с помощью масс-спектрометрии MALDI. . Масс спектр m/z (%): 404 (100%); 388 (70%); 246 (42%). Полученные значения для молекулярных ионов оказались неожиданно высокими, что позволило предположить о наличии сложных структур, включающих в себя Ag+, что в последующем было подтверждено качественной реакцией на ионы серебра. Однако для установления структуры полученных комплексных соединений требуются дополнительные исследования.
4. Охрана труда
Введение
Работа на химических производствах связана с использованием агрессивных жидкостей и газов, высоких температур и других опасных и вредных факторов, влияющих на организм человека, поэтому необходимо уделять большое внимание вопросам охраны труда и защиты окружающей среды. Под охраной труда понимают систему мероприятий, обеспечивающих безопасность, сохранение здоровья и работоспособность человека в процессе труда. Охрана труда является неотъемлемой частью производственной деятельности и должна обеспечиваться на всех стадиях технологического процесса. Особенно важно учесть все вредные факторы при работе химика-технолога, труд которого неизбежно связан с токсическими и пожароопасными веществами. В ходе разработки методов синтеза и анализа новых препаратов, создания новых технологий должны быть тщательно продуманы все меры предосторожности, позволяющие исключить воздействие на человека опасных и вредных производственных факторов, обеспечить снижение травматизма и профессиональных заболеваний, обеспечить охрану окружающей среды.
Проведение любой научно-исследовательской работы в химической лаборатории неразрывно связано с приобретением необходимых навыков безопасной работы, изучением и последовательным соблюдением норм и правил техники безопасности, заботой об улучшении и оздоровлении условий труда, что очень актуально в настоящее время.
Рассматриваемая магистерская диссертация, посвященная синтезу пиррольных интермедиатов для высоко сопряженных порфиринов, выполнена на кафедре ХТТОС МГАТХТ им. М.В.Ломоносова. Ниже анализируются токсичные и пожароопасные свойства веществ, использованных в работе, а также условия, при которых проводился эксперимент и необходимые меры по охране труда.
Токсические и пожароопасные свойства веществ.
Под токсичностью химических веществ подразумевают их способность вызывать нарушения нормальной жизнедеятельности, приводить к патологическим изменениям в организме или вызывать гибель живого организма. Для характеристики вредности вещества применяется система ПДК в воздухе рабочей зоны. Пожароопасность определяется тем, что в работе используются легковоспламеняющиеся и горючие жидкости. В настоящей работе использовались пожароопасные и токсичные вещества. Все работы с ними проводились в вытяжном шкафу при полном отсутствии огня.
Токсикологические характеристики, величины ПДК и пожароопасные свойства веществ, используемых в работе, приведены в таблицах 1,2.
Таблица 1. Токсические свойства веществ [85,86].
| Наименование вещества | Характер воздействия на организм | Меры и средства первой помощи | ПДК, мг/м3 | Класс опасности |
| 1 | 2 | 3 | 4 | 5 |
| Азотная кислота | Вызывает ожоги кожи, при вдыхании паров - удушье и кашель, при попадании внутрь - раздражение слизистых оболочек. | При ожогах кожи - промыть большим количеством воды. | 5 | III |
| Ацетон | Поражает нервную систему, наркотическое воздействие, оказывает влияние на функции почек. | При инголяционном отравлении - промывание глаз водой, ингаляция кислородом; при перорильном - промывание желудка. | 200 | IV |
| Ацетонитрил | Головная боль, апатия, тошнота. | Вдыхание амилнитрита. | 10 | Ш |
| Бензол Толуол | Действует на нервную систему, наркотик, снижает артериальное давление, нарушает дыхание, вызывает судороги, кровотечения в полости рта, влияет на состав крови, раздражает кожу. | Искуственное дыхание, при попадании в органы пищеварения вызвать рвоту и дать слабительное. | 20 | II |
| 1 | 2 | 3 | 4 | 5 |
| Гексан Гептан | Слабое воздействие на кожу, может вызвать временное опьянение. | Свежий воздух. | 250 350 | IV IV |
| Диметилсульфоксид | Малотоксичен. | При попадании на кожу промыть водой. | 20 | IV |
| Диэтиловый эфир | Наркотическое воздействие, слезотечение, возможно развитие токсического отека легких. | Свежий воздух. При попадании внутрь - промывание желудка, рвота. | 300 | IV |
| Изопропиловый спирт | Наркотик, влияет на зрение и центральную нервную систему. | Свежий воздух, горячее молоко с содой. | 100 | III |
| Метанол | Сильный нервный яд. При попадании внутрь вызывает потерю зрения, паралич дыхательных центров. | Промывание желудка водой, этанолом, высокое положение головы, лед на голову. Вдыхание кислорода с 5% углекислоты, искуственное дыхание. | 5 | III |
| Натрия гидроксид Калия гидроксид | Ожоги кожи и слизистых оболочек. | Промыть струей воды, обработать борной кислотой. | 0,5 0,5 | II II |
| Пиперидин | В больших дозах угнетает; вызывает отчетливую сосудистую реакцию с нарушением кровяного давления. | При остром раздражении слизистых оболочек глаз промыть 2% раствором соды или борной кислоты. В глаза закапать 0,5% раствор дикаина. | 0,2 | II |
| 1 | 2 | 3 | 4 | 5 |
| SiO2 | Общетоксическое действие, нарушение дыхательной функции легких (силикоз), раздражение легочной ткани острыми твердыми гранями частиц пыли. | Устранение пылеобразования, использование индивидуальных защитных средств (очки, респиратор). | 1 | II |
| Соляная кислота | Вызывает ожоги кожи, при вдыхании паров - удушье и кашель, при попадании внутрь - раздражение слизистых оболочек. | При ожогах кожи - промыть большим количеством воды, затем 5% раствором бикарбоната натрия; свежий воздух. | 5 | III |
| Уксусная кислота | Сильное раздражающее действие, хроническое воздействие паров вызывает острые, а затем хронические риниты, фарингиты, ларингиты, коньюктивиты и бронхиты. | Свежий воздух; промыть 2% раствором соды нос, глотку, рот, дать теплого молока с содой. При ожоге глаз - длительное промывание водой. | 5 | III |
| Уксусный ангидрид | Сильное раздражающее действие. | Промыть струей воды. | 20 | IV |
| Хлорид -кальция | При работе вызывает трещины на коже рук. | Промывание водой кожи рук. | 2,5 | III |
| 1 | 2 | 3 | 4 | 5 |
| Хлористый метилен | Поражает центральную нервную и кроветворную системы, вызывает патологические изменения печени и почек. | Искуственное дыхание, внутривенно - лобелин, бемегрид; при попадании внутрь - вызвать рвоту, дать слабительное, промывание желудка вазелиновым маслом, инголяция кислородом. | 20 | IV |
| Хлористый тионил | Вызывает раздражение слизистых оболочек дыхательных путей, глаз, легких, кожных покровов. | Свежий воздух, промывание водой, покой. | 0,5 | II |
| Хлороформ | Наркотический эффект, токсилогическое действие на обмен веществ, внутренние органы, особенно на печень. | Свежий воздух, искусственное дыхание, покой. | 200 | IV |
| Четырех-хлористый углерод | Наркотик, повреждение печени, почек, легких, потеря сознания, головная боль, головокружение, невриты зрительного нерва. | Покой, введение глюкозы, исскуственное дыхание, высококалорийная диета | 20 | II |
| Этанол | Действует на центральную нервную и сосудистую системы, печень; наркотик, вызывает тахикардию. | Промывание желудка, искусственное дыхание | 1000 | IV |
Таблица 2. Пожароопасные свойства веществ [86,87].
| Наименование веществ | Плотность пара по воздуху | Температура, 0С | |||||||||||
Пределы воспламенения
Вспышки
Воспламенения
Самовоспламенения
Температурные,0С
Концентрационные %
нижний
верхний
нижний
верхний
5
6
7
8
9
465
-20
6
2,9
13
> 450
3
---
4,1
---
340
40
65
---
---
634
-14
13
1,4
7,1
---
-26
4
1,2
7,5
202
---
---
1,1
6,7
215
---
---
2,8
---
164
-45
13
1,7
49
400
2
12
8
37
464
7
39
6
34,7
---
---
---
1,39
---
536
0
30
1,3
6,7
555
---
---
---
---
---
35
76
3,3
22
360
37
75
1,21
9,9
580
---
---
12
22
Пары CCl4 оказывают ингибирующее действие на горение многих органических веществ. Минимальная гасительная концентрация-10,5%, т.к. может содержать фосген не применяется в качестве огнегасительного средства.
18
404
11
41
3,6
Таблица 3. Обобщенный анализ потенциальных опасностей.
| Наименование технологичес-кой операции (ТО) | Оборудование на котором осуществля-лась ТО | Реактивы, использовав-шиеся при проведении ТО | Условия проведения ТО | Выявление опасности и вредности |
| Перегонка растворителя | Электричес-кая плитка, стеклянная посуда, термометр | Органические растворители | Зануление электрической плитки | Поражение электричес-ким током, термический ожог |
| Проведение реакций | Электронагреватель, маг-нитная и механическая мешалки, силиконовая баня | Органические растворители и вещества, кислоты, щелочи | В вытяж-ном шкафу, ис-пользова-ние термо-реле | Поражение электричес-ким током, термический или химичес-кий ожог, травмы при работе со стеклом |
| Фильтрование | Водоструйный насос, стеклянная посуда | Органические растворители, вещества | Вакуум | Травма стеклом |
| Хроматография | Колонка с сорбентом | Органические растворители, вещества | --- | Отравление парами растворителей |
| Экстракция | Стеклянная посуда | Органические растворители, вода, кислоты | Работа в вытяжном шкафу | Химические ожоги, травмы стеклом |
Обоснование мер предосторожности при проведении потенциально опасных операций.
1. При взвешивании аналитических эталонов рекомендуется:
§ обеспечить эффективную вентиляцию;
§ носить перчатки и лабораторный халат;
§ принимать меры для предотвращения вдыхания взвешенных частиц и контакта со ртом;
§ в случае загрязнения следует немедленно промыть кожу, одежду или загрязненную поверхность водой.
2. При работе с ЛВЖ необходимо соблюдать следующие меры предосторожности:
§ не допускать попадания горючих газов в атмосферу;
§ при проведении процессов, связанных с нагреванием, пользоваться эффективными водяными холодильниками;
§ работу проводить в круглодонных колбах из тугоплавкого стекла;
§ диэтиловый эфир способен при хранении образовывать взрывоопасные перекиси. С целью удаления перекисных соединений проводить очистку растворителя пирогаллолом;
§ во избежание разлива ЛВЖ и возгорания, большие количества растворителей переливать без плесканий, пользуясь специальной воронкой.
3. При работе с кислотами и щелочами следует пользоваться резиновыми перчатками и защитными очками, так как эти вещества могут вызвать ожоги кожи. При попадании растворов кислот и щелочей на кожу пораженное место нужно промыть струей холодной воды и обработать раствором соды (при попадании кислоты) или борной кислоты (при попадании щелочи).
4. Работа с вакуумом требует соблюдения следующих мер предосторожности:
§ не использовать в установках плоскодонные колбы и склянки, кроме специально предназначенных для работы при пониженном давлении;
§ использовать для работы приборы, изготовленные из специального молибденового стекла;
§ проверять используемую стеклянную посуду на наличие видимых дефектов (трещин, пузырей и др.).
5. В работе использовались различные электроприборы: нагреватели, магнитные мешалки, весы, роторный испаритель.
Основными мерами предотвращения поражений электрическим током в лаборатории являются защита от прикосновения к находящимся под напряжением частям электрооборудования и применение защитного заземления.
Электробезопасность.
Лаборатория кафедры ХТТОС МГАТХТ им. М.В.Ломоносова по классификации помещений по степени опасности поражения электрическим током относится к помещениям без повышенной опасности, так как помещение сухое (с влажностью не более 60%), с нормальной температурой не выше 25о С, с изолированными полами (линолеум) [88,89].
При использовании в лабораторной работе электроустановок запрещалось:
§ вскрывать электроплитки;
§ проводить включение электроприборов вблизи ЛВЖ;
§ применять для подключения электропотребителей проводники с поврежденной изоляцией;
§ оставлять включенные приборы без присмотра.
При работе в лаборатории использовались следующее электрооборудование: электронагреватели, магнитные и механические мешалки, роторный испаритель, прибор для определения температуры плавления. При их применении контролировались: наличие защитного зануления, наличие заземления, исправность оборудования, соответствие напряжения в сети напряжению для данного прибора.
Оборудование в лаборатории было снабжено защитным занулением, при этом части электроустановок присоединялись к многократно заземленному нулевому проводу, а для снятия статического электричества-заземлением. Была предусмотрена система тройных тумблеров для включения оборудования в электрическую сеть.
Для обеспечения электробезопасности не применялись плитки с открытой спиралью, которые могли бы привести к аварийной ситуации.
Санитарно-гигиенические условия.
Помещение, в котором выполнялась экспериментальная часть магистерской диссертации, характеризовалось малым тепловыделением, работа классифицировалась как легкая [89].
Работа с токсическими и взрывопожароопасными веществами проводилась под тягой, лаборатория была оснащена двумя вытяжными шкафами. Скорость воздуха под тягой в соответствии с паспортными данными составляла не менее 0,7 м/сек., что обеспечивает унос вредных паров с поверхности жидкости. Нормальные санитарно-гигиенические условия в лаборатории обеспечивались нормальной работой приточно-вытяжной вентиляции с кратностью обмена воздуха 2,5.
В лаборатории имелась аптечка медицинская с комплектом средств для оказания первой помощи.
Проводимая в лаборатории работа не требует высокой точности, коэффициент естественной освещенности не менее 1% на самом удаленном от окна рабочем месте. Естественное освещение в лаборатории - боковое. Коэффициент естественной освещенности по СНиП II-4-79 - 1,5. Естественное освещение дополняется искусственным, которое обеспечивается на местах люминесцентными лампами. Освещенность на рабочем месте составляет не менее 100 лк.
Во время выполнения экспериментальной работы образовывались отходы, которые можно разделить на органические и неорганические, жидкие и газообразные. Перед сливом неорганические отходы нейтрализовывали, многократно разбавляли водой и сливали в канализацию. Органические жидкие отходы по возможности регенирировали, перегоняя их, и использовали повторно. Если это было неосуществимо, то отходы собирали в специальные емкости, которые затем уничтожали в общеинститутских масштабах. Условия труда в лаборатории соответствовали санитарным нормам [86,90].
Пожарная опасность в лаборатории и средства пожаротушения.
Необходимые для повседневной работы ЛВЖ и ГЖ (суточная норма не более 1 л) хранились в плотно закрывающихся металлических ящиках, выложенных изнутри асбестом. Концентрированные кислоты и щелочи-в вытяжных шкафах на специальных полках. Реактивы, нестойкие при комнатной температуре, хранились в холодильнике.
Хранение в лаборатории разных групп реактивов требует обязательного соблюдения порядка их совместного хранения.
В соответствии с ОНТП 24-86 лаборатория относится к категории "В", так как работа проводится с большим количеством жидкостей, имеющих температуру вспышки ниже 28 оС, которые не могут, однако, образовывать взрывоопасные концентрации во всем объеме лаборатории [88].
По взрывоопасности в соответствии с ПУЭ лаборатория относится к классу "В-1б", так как имеющиеся в помещении горючие газы и легковоспламеняющиеся жидкости используются в небольших количествах, без применения открытого пламени, и работа с ними проводится в вытяжных шкафах [91].
Группа взрывоопасной смеси паров жидкостей, используемых в работе, по ПИВРЭ соответствует Т1 (температура самовоспламенения горючих веществ более 450 оС.)
Из средств пожаротушения в лаборатории имеются углекислотный огнетушитель, песок, асбестовое одеяло. Из средств индивидуальной защиты в лаборатории есть защитные очки и экраны, резиновые перчатки и фартук, противогаз марки ГП-5, аптечка.
Экспериментальная часть.
Для идентификации синтезируемых соединений и контроля протекания реакций использовали ТСХ на пластинах “Silufol UV 254” в различных системах растворителей. Проявляли в парах йода или нагреванием до 120-1400 в течение 2-3 минут или под УФ-лампой. Спектры H1- и C13-ЯМР растворов анализируемых веществ снимали на спектрометрах “Bruker 200SY”(Германия) с рабочей частотой 200Мгц и 50 Мгц соответственно, и “Bruker DPX300”(Германия) с рабочей частотой 300Мгц и 75 Мгц соответственно. ИК-спектры в вазелиновом масле и тонком слое вещества снимали на спектрофотометре “Shimadzu IR‑435”(Япония). Масс-спектры снимали на масс-спектрометрах “Finnigan MAT INCOS 50”, метод- электронный удар 70 эВ и “Kratos PC-Kompact MALDI 4”, метод- испарение лазером. Температуру плавления определяли с помощью прибора для определения температуры плавления “Boetius” (Германия). Колоночную хроматографию проводили на силикагеле фирмы Merck Silica gel 60, использовали растворители с характеристиками ХЧ, ОСЧ или Dried.
Метил–2,4–пентандион (41).
В трехгорлую колбу на 250 мл, снабженную термометром, обратным холодильником, мешалкой и воронкой для сыпучих веществ, вносят 108 мл абсолютного этанола и добавляют порциями 8,5 г (0,37 моль) Na до растворения. Воронку для сыпучих веществ заменяют на капельную воронку. Образовавшийся этилат натрия нагревают до 450 и добавляют по каплям при той же температуре 38 мл (0,37 моль) 2,4‑пентандиона. Полученный раствор охлаждают до 35‑400 и прибавляют по каплям 23 мл (0,37 моль) CH3I, таким образом, чтобы температура реакционной массы не превышала 400. Реакционную массу перемешивают в течение 1 часа при 350, затем спирт отгоняют, выпавший осадок NaI растворяют минимальным количеством воды, слои разделяют и водный слой экстрагируют диэтиловым эфиром. Эфирную вытяжку сушат MgSO4. Эфир отгоняют, а остаток перегоняют в вакууме. Получают 20,3 г (48 %) 3‑метил‑2,4‑пентандиона (41).
nD22=1.4440 Ткип=67–680/20–23 мм.
Лит.: nD20=1.4420 Ткип=172–1740 [92].
Дата: 2019-05-28, просмотров: 450.