Рассмотрим зависимость плотности тока j газообразного диэлектрика от напряженности электрического поля в широком интервале E (рисунок 3.5). На участке ОАБ наблюдается несамостоятельная электропроводность, а на участке БВ – самостоятельная. В слабых электрических полях до значения E=Eн плотность тока линейно возрастает с увеличением напряженности поля. Следовательно здесь выполняется закон Ома. На участке ОА по мере роста напряженности поля плотность тока растет, так как увеличивается число ионов и электронов, участвующих в его образовании. Часть электронов уносится к электродам, часть рекомбинируется. По мере возрастания приложенного напряжения ионы уносятся к электродам сильнее, все меньше успевая рекомбинировать, и начиная с E  Eн, рекомбинация становится практически равной нулю. С этого момента (участок АБ) все образующиеся под действием внешнего энергетического воздействия ионы и электроны будут разряжаться на электродах, обуславливая ток насыщения jн, который при дальнейшем увеличении Е остается постоянным.
Eн, рекомбинация становится практически равной нулю. С этого момента (участок АБ) все образующиеся под действием внешнего энергетического воздействия ионы и электроны будут разряжаться на электродах, обуславливая ток насыщения jн, который при дальнейшем увеличении Е остается постоянным.
Самостоятельная электропроводность возникает в области сильных полей. Возрастание тока при E  Eкр (участок БВ) обусловлено увеличением числа носителей заряда (электронов и ионов) в результате электронной ударной ионизации, и эмиссии электронов с катода. При Eпр возникает пробой, в этом состоянии газ утрачивает свои электроизоляционные свойства, так как между электродами образуется плазменный газоразрядный канал проводимости.
Eкр (участок БВ) обусловлено увеличением числа носителей заряда (электронов и ионов) в результате электронной ударной ионизации, и эмиссии электронов с катода. При Eпр возникает пробой, в этом состоянии газ утрачивает свои электроизоляционные свойства, так как между электродами образуется плазменный газоразрядный канал проводимости.
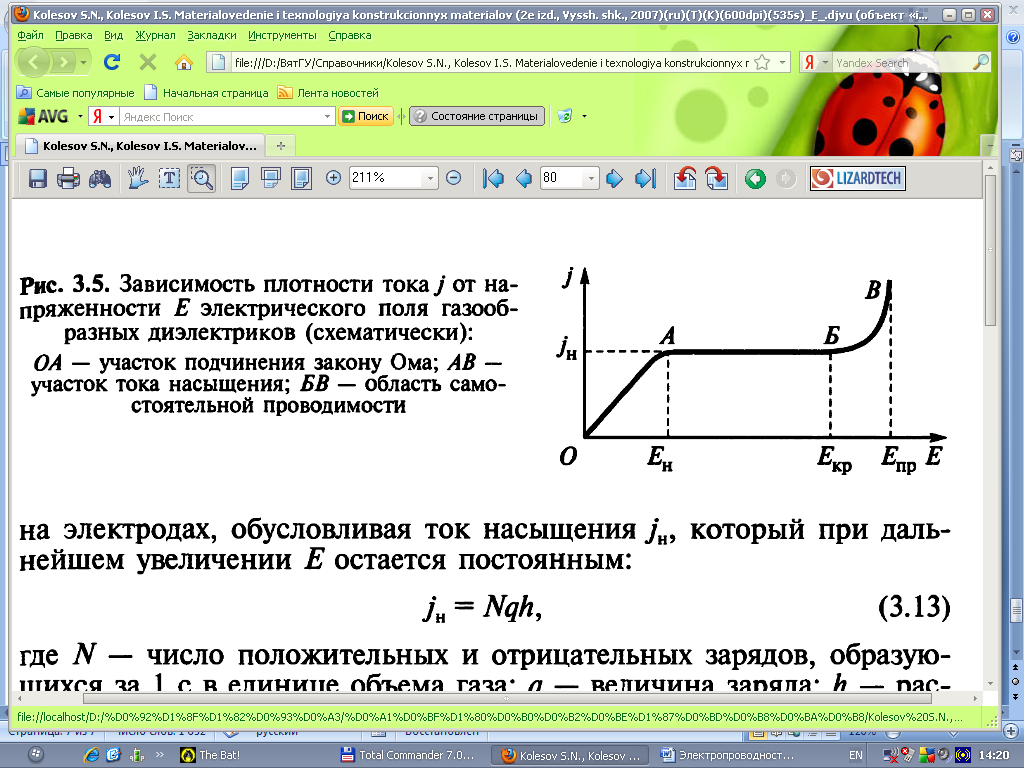
Таким образом, на основании представленной зависимости, мы сделали заключение о том, что электропроводность газов обуславливается наличием свободных зарядов, которые возникают в результате действия внешних ионизаторов.
ЭЛЕКТРОПРОВОДНОСТЬ ЖИДКИХ ДИЭЛЕКТРИКОВ
В жидких диэлектриках наблюдаются в основном ионная и электрофоретическая проводимости. В области сильных электрических полей к этим видам проводимости добавляется электронная составляющая.
Ионная проводимость
Ионная проводимость обусловлена дрейфом — направленным движением положительных и отрицательных ионов под действием приложенного электрического поля и разряжением их на электродах. Ионы образуются в результате электролитической диссоциации (распада) ионогенных веществ (ионной примеси) под действием полярных молекул среды (растворителя). Ионогенная примесь между атомами (ионами) имеет химическую связь: ионную (например, NaCl) или ковалентную, сильно полярную (например, Н2О).
Если примесь имеет ионную связь (например, NaCl), то механизм электролитической диссоциации выглядит так, как показано на рис. 3.6. Полярные молекулы растворителя (внешней среды) притягиваются ионами, находящимися в узлах кристаллической решетки, ориентируются возле этих ионов и, в свою очередь, притягивают их к себе. Притягивая ионы решетки к себе, молекулы растворителя ослабляют связь между ними, в результате чего ионы отделяются от решетки и переходят в растворитель. Переходящие в растворитель ионы остаются связанными с его полярными молекулами.
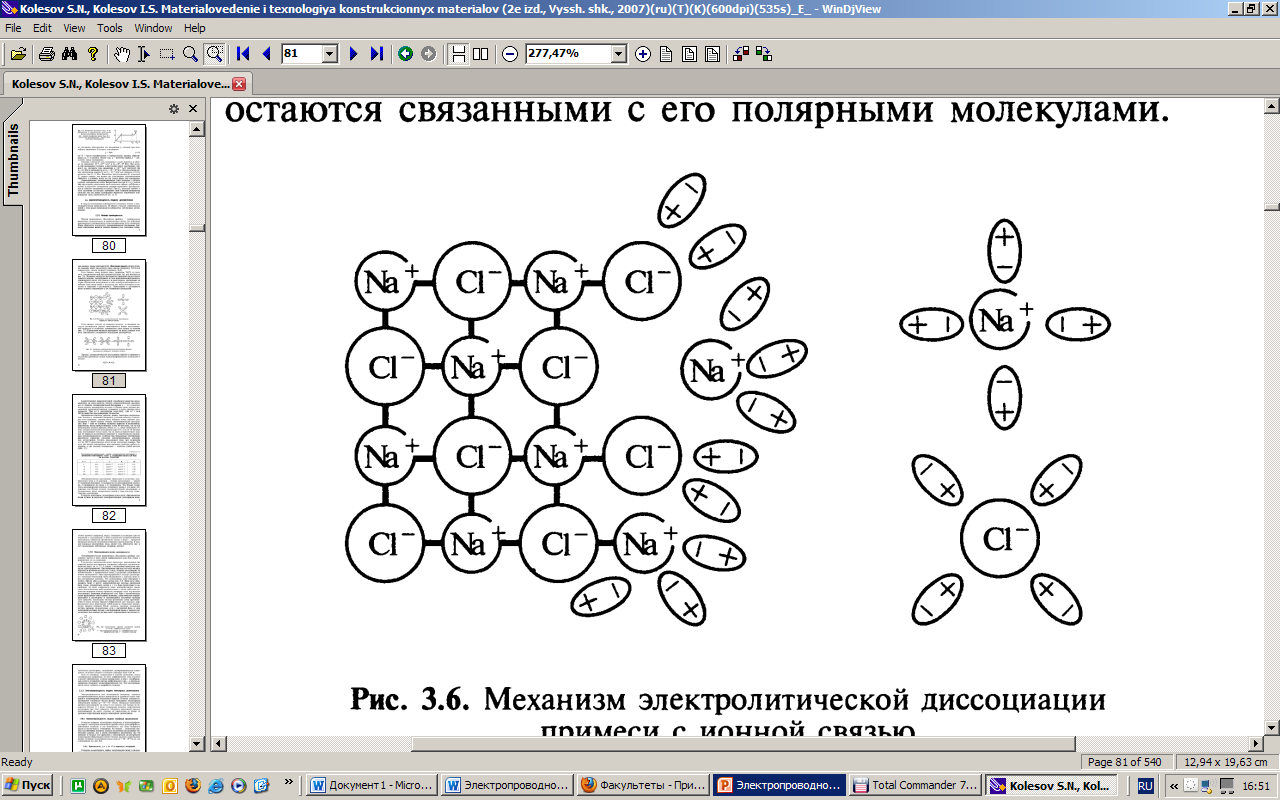
Рис. 3.6. Механизм электролитической диссоциации примеси с ионной связью
Если примесь состоит из полярных молекул, то полярные молекулы растворителя (среды) ориентируются вокруг диссоциируемой молекулы и ослабляют ковалентную связь между ее атомами (рис. 3.7). В результате молекула распадается на ионы, которые остаются связанными с полярными молекулами растворителя.

Рис. 3.7. Механизм электролитической диссоциации примеси, состоящей из свободных полярных молекул
Процесс электролитической диссоциации обратим и приводит к состоянию равновесия между недиссоциированными молекулами и ионами

Электролитическая диссоциация происходит в отсутствие электрического поля, а ее величина - степень диссоциации - зависит от следующих факторов:
1) полярности ( 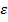 ) диссоциируемой молекулы,
) диссоциируемой молекулы,
2) полярности ( 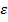 ) среды,
) среды,
3) температуры.
Чем больше полярность диссоциируемых молекул, полярность среды и чем выше температура, тем больше степень электролитической диссоциации и, следовательно, выше концентрация ионов и ниже удельное сопротивление диэлектрика.
В жидких неполярных диэлектриках ионы могут образовываться двумя путями: в результате электролитической диссоциации ионогенной примеси (например, воды), попавшей в диэлектрик при его получении и эксплуатации, а также в результате электролитической диссоциации свободных органических кислот и воды - продуктов термоокислительной деструкции (старения) самого вещества. В жидких полярных диэлектриках ионы, кроме того, образуются еще за счет диссоциации собственных полярных молекул.
Дата: 2019-02-25, просмотров: 393.