Виды химических связей в веществах, применяемых при создании материалов.
В веществах различают три основных типа химических связей: ковалентную, металическую и молекулярную (Вандервальса). Ковалентная связь представляет собой связь, образованную за счет спаривания валентных электронов средних атомов и прикрытия электронных оболочек. Главным представителем вещества обладающим ковалентной связью - водород. Металическая связь: данный вид связи присутствует в системах, состоящих из положительных атомов, находящихся в среде обобществленных электронов, которые представляют собой электронный газ. При этом целостность вещества обусловлена притяжением между положительными атомами и отрицательными электронам. По сравнению с ковалентной связью, металлическая связь характеризуется меньшей энергией и из-за больших межатомных расстояний вещества обладающие металлической связью обладают большей пластичностью. Ионная связь: вид химической связи присутствует в веществах, вмещающих металлические и металлоидные атомы. При данном виде химической связи происходит переход валентных электронов от металлического атома к металлоидному и возникновению электростатического притяжения. Данный вид химической связи характерен для ионов кристаллов. Молекулярная связь (Вандервальса): данный вид химической связи наблюдается в ряде веществ между молекулами, имеющими ковалентный характер внутри молекулярного взаимодействия. При этом возникает межмолекулярное притяжение, обусловленное согласованным движением валентных электронов в соседних молекулах. Благодаря этому движение возникает система связанных электрических дифурий. Схема образования межмолекулярных связей:
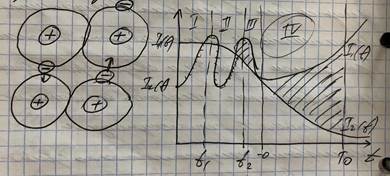 |
Тела, обладающие молекулярной связью, как правило, представляют из себя кристаллы углеводорода или кристаллы инертных газов.
Стекла и аморфные вещества.
В отличие от веществ, имеющих кристаллическую структуру, стеклообразные вещества, характеризуются наличием ближнего порядка атомов и отсутствием дальнего.
Физические процессы и явления в проводниковых материалах.
Проводящие материалы могут находиться в жидком, твердом или газообразном состоянии. К твердым проводящим материалам относят металлы, металлические сплавы, и неметаллические проводящие материалы. Жидкие проводники представляют собой электролиты или расплавленные металлы. Газообразными приводящими материалами могут быть ионизированные газы. Металлы, находящиеся в твердом и жидком состоянии обладают электронным типом проводимости и называют проводниками первого рода. Проводниками второго рода называют проводящие вещества обладающие ионным типом проводимости.
Понятие термо ЭДС.
В случае соединения двух различных проводников, образующих замкнутую цепь, образуется термоэлемент, называемый термопарой. Между металлами, в кадкой из точек соединения возникает внутренняя контактная разность потенциалов. При различной температуре контактов в цепи возникает электрический ток. В случае, если провести разрыв этой электрической цепи, то между точками разрыва возникнет разность потенциалов , называемой термо ЭДС. Это явление получило название: эффект Зеебека. Величина термо ЭДС экспериментально оказалась пропорциональна разности температур между точками соединения контактирующих проводников.
Здесь альфа ав это коэффициент пропорциональности, называемый относительной дифференциальной термо ЭДС.
UAB=альфаАВ(Т2-Т1)
Величина относительной дифференциальной термо ЭДС, определяется разностью абсолютных термо ЭДС, находящихся в контакте проводников.
альфаАВ=альфаА-альфаВ
Величина абсолютной термоЭДС для металла , определяется формулой:
альфаА=(pi2/3)(k/e)kT/ЭF
———————————————————————————————————————————————————
М2
16.10.2018
Лекция №7.
Примесные полупроводники.
В приметных полупроводниках связи с наличием в их составе примесей в случае если их концентрация не слишком велика в запрещенной зоне формируются дискретные энергетические уровни, называемые приметными, при этом поскольку концентрация примесей не велика, не происходит формирование сплошных энергетических зон. В зависимости от расположения приметных атомов, различают примеси замещения и примеси внедрения. В примесях замещения, примесный атом располагается в узлах кристаллической решетки, а в примесях внедрения примесный атом располагается в междуузлии.
23.10.2018
Лекция№8.
Механизмы поглощения света.
1). Собственное поглощение света.
При реализации данного механизма, энергия фотонов расходуется на ионизацию собственных атомов полупроводника. Интенсивность собственного поглощения света определяется длиной волны излучения и шириной запрещенной зоны. Соотношение между шириной запрещенной зоны и частотой излучения определяет пороговую длину волны, при которой может реализоваться механизм собственного поглощения.
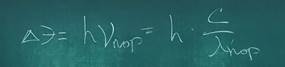 |
Экситонное поглощение.
При реализации данного механизма поглощения в полупроводнике образуется квазичастицы, называемые экситонами. Экситон представляет собой систему электростатически связанных между собой электрона и дырки. Величина энергии, необходимая для образования экситона в несколько раз меньше ширины запрещенной зоны. В результате появления экситона происходит их перемещение по структуре полупроводника, при этом поскольку частица в целом электрически нейтральна тоне приводит к изменению электропроводности.
Поглощение света примесями.
В случае реализации данного механизма энергия светового излучения расходуется на ионизацию примесных атомов, в результате чего-либо происходит переход электронов с донорных уровней зоны проводимости, либо переход дырок с акцепторах уровней в валентную зону.
Понятие фотопроводимости.
Фотопроводимостью называют изменение электрической проводимости и удельного сопротивления вещества под действием светового излучения. Величина фотопроводимсти дельта гамма, определяется как разность проводимости полупроводника под действием света и в темноте.
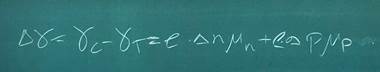 |
В случае если происходит оптическая генерация, то она характеризуется скоростью генерации, определяемой соотношением: 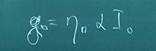
Квантовым выходом внутреннего фотоэффекта называют число пар неравновесных носителей зарядов, образовавшихся в результате поглощение одного фотона.
Понятие люминесценции .
Люминесценцией называют электромагнитное не тепловое излучение, обладающее длительностью значительно превышающей период световых колебаний. В зависимости от вида возбуждения различают фотолюминисценцию, катодолюминисценцию, т.е. люминесценцию под воздействием пучка электродов, и магнитную люминесценцию, под действие электромагнитного поля.
Ионная поляризация.
При реализации данного механизма поляризации под действием электрического поля происходит упругое смещение ионов, находящихся в узлах кристаллической решетки, на расстояние, меньшее периода кристаллической решетки. Данный механизм поляризации также является быстрым и время его установления составляет порядка 10-13 секунды. Данных механизм поляризации также не сопровождается диэлектрическими потерями и характерен для веществ, обладающих ионным строением. Электронная и ионная поляризации относятся к группе быстрых механизмов поляризации, которые характеризуются отсутствием диэлектрических потерь.
Резонансная поляризация.
Данный механизм поляризации наблюдается в диэлектриках на световых частотах, при совпадении частоты внешнего поля с собственной частотой колебаний атомов или электронов.
Миграционная поляризация.
Данный механизм поляризации наблюдается в диэлектриках, в составе которых присутствуют макроскопические проводящие включения. При этом под действием внешнего электрического поля положительные и отрицательно заряженные частицы перераспределяются по объему примеси, из-за чего появляется электрический момент.
Доменная поляризация.
Так же иногда называется спонтанной или самопроизвольной поляризацией. Данный механизм поляризации присутствует в веществах с особым строением, характеризующимся наличием макроскопических областей, называемых доменами, которые обладают электрическим моментом даже в отсутствии внешнего электрического поля. 
При этом суммарный электрический момент в отсутствии электрического поля равен нулю, а под действием электрического поля происходит переориентация электрического момента и разрастание доменов, электрический момент которых сонаправлен действию электрического поля.

Частотная зависимость диэлектрической проницаемости:
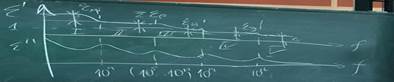 |
На данном графике приведены частотные зависимости для действительной и мнимой части комплексной диэлектрической проницаемости, которые показывают характер изменения диэлектрической проницаемости в зависимости от реализующихся механизмов поляризации. На самых низких частотах успевают пройти все механизмы поляризации, при этом каждый из них вносит свой вклад в суммарную величину диэлектрической проницаемости. На самых низких частотах могу быть реализованы все механизмы поляризации, включая медленные, при более высоких частотах, за период электрического поля медленный механизм поляризации не успевает установиться и, соответственно, не оказывает влияние на итоговую величину диэлектрической проницаемости. На первом участке присутствуют все механизмы поляризации, включая миграционную. На втором участке основной вклад вносят релаксационные механизмы поляризации. Третий участок характеризуется наличием ионной поляризации. На участке 4 успевает протекать только электронная поляризация. И при крайне высоких частотах поляризация не успевает происходить и действительная составляющая диэлектрической проницаемости стремится к единице.
Ионные диэлектрики.
К ним преимущественно относятся твердые неорганические диэлектрики обладающие ионной, ионно-релаксационной, электронной и электронно-релансационной поляризацией.
Потери в диэлектриках.
Диэлектрическими потерями называют электрическую мощность, затрачиваемую на нагрев диэлектрика, находящегося в электрическом поле. Потери при этом обусловлены как нагревом диэлектрика, обусловленным протеканием тока сквозной проводимости, так и потерями при протекании поляризационных токов. На практике величину потерь в диэлектрике характеризуют углом диалектических потерь delta, который представляет собой угол, дополняющий до 90о, угол сдвига фаз между током и напряжением в емкостей цепи. На практике также используется величина tg(delta), поскольку эта величина прямо входит в формулу для расчета величины диэлектрических потерь.
Параллельная и последовательная эквивалентная схема для диэлектрика, обладающего потерями и векторные диаграммы напряжений и токов: 
В представленных на рисунках последовательных и параллельных эквивалентных схемах величина tgδ определяется, соответственно, как отношение токов для параллельной схемы и отношение напряжений для  последовательной схемы:
последовательной схемы:
В случае качественного диэлектрика величина выделяемой на нем мощности определяется следующим выражением: 
В случае если на потери в конденсаторе наибольшее влияние оказывает значение активного сопротивления самих обкладок конденсатора, подводящих проводов, то величина рассеиваемой мощности пропорциональна квадрату частоты протекающего тока и величине активного сопротивления: 
В общем случае диэлектрическая проницаемость диэлектрика, характеризующегося потерями, является комплексной величиной, которая определяется следующим соотношением: 

Величина tgδ также может быть определена как отношение мнимой и действительной составляющей комплексной диэлектрической проницаемости: 
Наличие диэлектрических потерь в диэлектрике обуславливает комплексный характер величины диэлектрической проницаемости, при этом наличие потерь характеризует именно мнимая составляющая.
Виды химических связей в веществах, применяемых при создании материалов.
В веществах различают три основных типа химических связей: ковалентную, металическую и молекулярную (Вандервальса). Ковалентная связь представляет собой связь, образованную за счет спаривания валентных электронов средних атомов и прикрытия электронных оболочек. Главным представителем вещества обладающим ковалентной связью - водород. Металическая связь: данный вид связи присутствует в системах, состоящих из положительных атомов, находящихся в среде обобществленных электронов, которые представляют собой электронный газ. При этом целостность вещества обусловлена притяжением между положительными атомами и отрицательными электронам. По сравнению с ковалентной связью, металлическая связь характеризуется меньшей энергией и из-за больших межатомных расстояний вещества обладающие металлической связью обладают большей пластичностью. Ионная связь: вид химической связи присутствует в веществах, вмещающих металлические и металлоидные атомы. При данном виде химической связи происходит переход валентных электронов от металлического атома к металлоидному и возникновению электростатического притяжения. Данный вид химической связи характерен для ионов кристаллов. Молекулярная связь (Вандервальса): данный вид химической связи наблюдается в ряде веществ между молекулами, имеющими ковалентный характер внутри молекулярного взаимодействия. При этом возникает межмолекулярное притяжение, обусловленное согласованным движением валентных электронов в соседних молекулах. Благодаря этому движение возникает система связанных электрических дифурий. Схема образования межмолекулярных связей:
 |
Тела, обладающие молекулярной связью, как правило, представляют из себя кристаллы углеводорода или кристаллы инертных газов.
Дата: 2019-02-02, просмотров: 370.