От количества растворённого в пластовой нефти газа зависят все её важнейшие свойства: вязкость, сжимаемость, термическое расширение, плотность и другие.
Распределение компонентов нефтяного газа между жидкой и газообразной фазами определяется закономерностями процессов растворения. Способность газа растворяться в нефти и воде имеет большое значение на всех этапах разработки месторождений от добычи нефти до процессов подготовки и транспортировки.
Сложность состава нефти и широкий диапазон давлений и температур затрудняют применение термодинамических уравнений для оценки газонасыщенности нефти при высоких давлениях.
Процесс растворения для идеального газа при небольших давлениях и температурах описывается законом Генри:
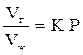 или
или 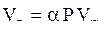 (2.38)
(2.38)
где Vг – объём растворённого газа при данной температуре;
К – константа Генри (К = f(a));
a – коэффициент растворимости газа;
Vж – объём жидкости-растворителя;
Р – давление газа над поверхностью жидкости.
Коэффициент растворимости газа (a) показывает, какое количество газа (Vг) растворяется в единице объёма жидкости (Vж) при данном давлении:
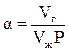 . (2.39)
. (2.39)
Коэффициент растворимости зависит от природы газа и жидкости, давления, температуры.
Природа воды и природа углеводородов различны. Углеводородная составляющая нефтяного газа растворяется хорошо в УВ системах, в нефти, а в воде хуже.
Неуглеводородные компоненты нефтяного газа, такие как СО, СО2, Н2S, N2, растворяются лучше в воде. Например, пластовая вода сеноманского горизонта Западной Сибири очень газирована, она содержит приблизительно 5 м3 углекислых газов на 1 тонну пластовой воды.
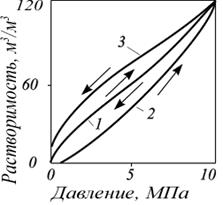
Растворимость углеводородов в нефти подчиняется закону Генри при низких давлениях. С повышением давления растворимость углеводородного газа растёт (рис. 2.5) до определённого давления.
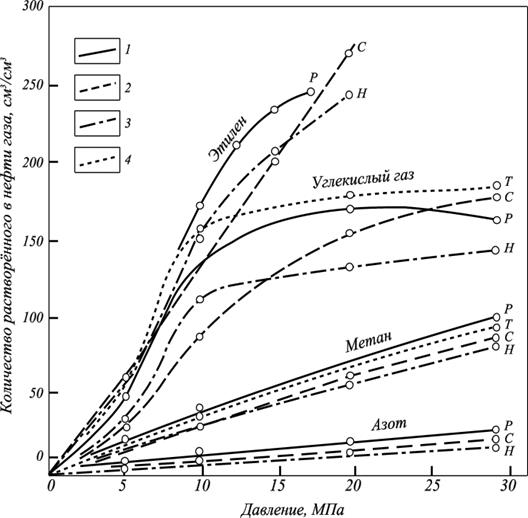
Рис. 2.5. Изотермы растворимости газов в нефти при температуре 50 оС:
1 – ромашкинская (Р); 2 – сураханская (С); 3 – небитдагская (Н);
4 – туймазинская (Т), по данным Т.П. Сафроновой и Т.П. Жузе
Из анализа представленных зависимостей следует, что растворимость газов в нефти, помимо давления, температуры и природы газа, зависит также от свойств нефти. Установлено, что разница в абсолютных величинах растворимости газов в исследованных нефтях и характер изотерм растворимости связаны с их различными фракционными и углеводородными составами. Растворимость углеводородных газов в нефти увеличивается с повышением содержания в ней парафиновых УВ. Работает принцип подобия: подобное растворяется в подобном. Туймазинская и ромашкинская нефти содержат во фракциях, выкипающих до 300 °С, около 52 % парафиновых углеводородов; в сураханской и небитдагской нефтях их содержится 42–43 %.
На степень растворения углеводородных газов больше влияет не молекулярная масса растворителя, а его природа.
При высоком содержании ароматических углеводородов в нефти растворимость в ней углеводородных газов ухудшается.
Разные компоненты нефтяного газа обладают различной растворимостью в нефтяных системах. С увеличением молекулярной массы газового компонента коэффициент растворимости его в углеводородных системах возрастает.
Форма изотерм растворимости для различных газов также не одинакова. Для плохо растворимых газов (N2, СН4) они характеризуются пологим подъёмом, почти равномерным во всем интервале давления.
То есть плохо растворимые газы лучше подчиняются закону Генри, чем хорошо растворимые. Изотермы хорошо растворимых газов (СО2, С2Н6, С3Н8) характеризуются резким подъёмом до определенных давлений, а затем зависимости выполаживаются. Последние обстоятельства объясняются обратными процессами растворения компонентов нефти в сжатом газе при высоких давлениях. Этот эффект в ряду углеводородных газов усиливается с ростом молекулярной массы газа. Для азота он незначителен, а при растворении метана в нефти обратное испарение наблюдается лишь при очень высоких давлениях.
Получение зависимостей концентрации углеводородных газов в нефтяных системах от давления затруднено не только отклонением поведения реальных газов от законов идеальных систем, но и увеличением объёма жидкости при введении в неё газа. Кроме того, значительное влияние на растворимость углеводородных газов оказывают процессы обратного испарения.
Количество выделившегося из нефти газа зависит не только от его содержания в нефти, но и от способа дегазирования. Различают контактное разгазирование, когда выделившийся газ находится в контакте с нефтью, и дифференциальное разгазирование, когда выделившийся из нефти газ непрерывно отводится из системы. Строгое соблюдение условий дифференциального дегазирования в лабораторных условиях затруднено, поэтому этот процесс заменяют на ступенчатое дегазирование, используя многократное (ступенчатое) разгазирование.
В процессе добычи нефти встречаются оба способа дегазирования. В начальные периоды снижения давления от давления насыщения, когда газ ещё неподвижен относительно нефти, происходит контактное разгазирование. В последующий период, по мере выделения газа из нефти, газ быстрее движется к забою скважины и можно говорить о дифференциальном разгазировании.
Коэффициент разгазирования определяется как количество газа, выделившегося из единицы объёма нефти при снижении давления на единицу. Коэффициент разгазирования при контактном способе разгазирования будет меньше, чем при дифференциальном способе разгазирования. При дифференциальном способе разгазирования нефти количество газа, остающегося в растворённом состоянии (условия по давлению разгазирования одинаковые), будет больше, чем при контактном способе (рис. 2.6).
Это связано с преимущественным переходом в паровую фазу метана в начале процесса дегазации. С удалением метана из системы при дифференциальном способе разгазирования нефти в паровой фазе увеличивается содержание тяжелых углеводородов (С2, С3, С4), что вызывает повышение растворимости их в нефти.
С повышением температуры растворимость углеводородных составляющих газа в нефти ухудшается.
Растворимость углеводородов в воде подчиняется закону Генри, но вид зависимости нелинейный.
|
Например, из эксперимента известно, что при давлении 3,5 МПа и температуре 35 °С нефтяной газ растворяется в воде (Vг/Vж) в количестве = 1 м3/м3. При повышении давления в 10 раз до 35 МПа растворимость газа увеличилась всего в 4 раза и составляет 4 м3/м3.
С увеличением давления возрастает растворимость солей в воде, то есть увеличивается минерализация воды. При увеличении минерализации (М), растворимость углеводородных газов в воде уменьшается (рис. 2.7).
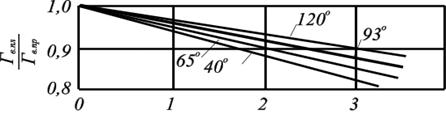
Общее содержание солей в пластовой воде, %·10–6
Рис. 2.7. Изменение растворимости природного газа в воде
в зависимости от минерализации
И это также является одним из факторов отклонения зависимости растворимости углеводородов в воде от линейного вида.
На практике растворимость углеводородного газа (м3/м3) в минерализованной воде оценивают по различным эмпирическим формулам, одна из которых приведена ниже:
aпл вод = aпресн вод·(1 – k·М), (2.40)
где aпл вод – растворимость нефтяного газа в пластовой воде;
aпресн вод – растворимость нефтяного газа в пресной воде;
k – поправочный коэффициент на минерализацию в зависимости от температуры (табл. 2.5);
М – содержание солей, %.
Таблица 2.5
Дата: 2018-12-21, просмотров: 466.