· Замещение галогенов
Более активные галогены вытесняют из галогенводородов и галогенидов металлов менее активные:
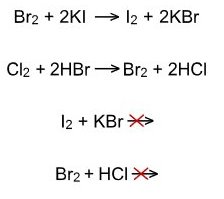
· Бром и йод вытесняют серу из сероводорода или из растворов солей:
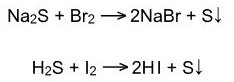
Хлор является более сильным окислителем, поэтому оксиляет серу из сульфид иона до серной кислоты:
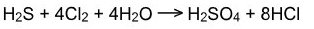
· Взаимодействие с водой:
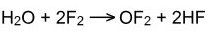
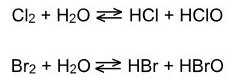
Йод не реагирует.
· Взаимодействие с щелочами:

Хлор и бром с холодным раствором щелочи:
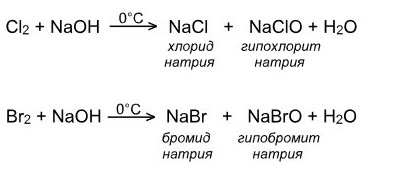
Хлор и бром с горячим раствором щелочи:
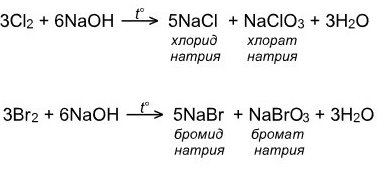
Йод реагирует только по второму варианту:

ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ
Реагирует как с простыми , так и со сложными веществами. Проявляет и окислительные, и восстановительные свойства.
Окислительные свойства проявляет в реакциях с металлами и с менее электроотрицательными неметаллами (водород, углерод, фосфор):
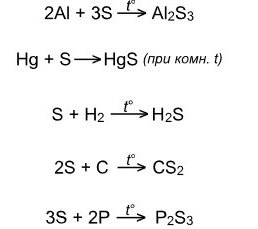
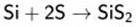
В роли восстановителя сера выступает в реакциях с более электроотрицательными неметаллами (см реакции с галогенами), а также со сложными веществами окислителями:
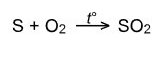
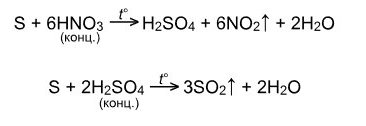
С щелочами при нагревании диспропорционирует:
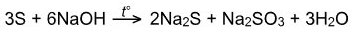
ХИМИЧЕСКИЕ СВОЙСТВА АЗОТА
Азот в свободном состоянии инертен из за тройной связи между атомами N≡N
1. Взаимодействие с металлами:
Ввиду своей значительной инертности азот при обычных условиях реагирует только с литием:
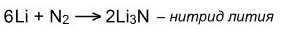
С щелочными и щелочноземельными реагирует при нагревании:
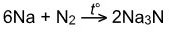
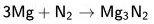
Взаимодействие азота с неметаллами
· Реагирует с водородом. Реакция обратимая:
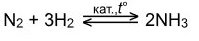
· Реагирует со фтором и кислородом, проявляя восстановительные свойства:
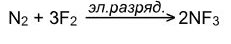
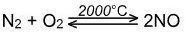
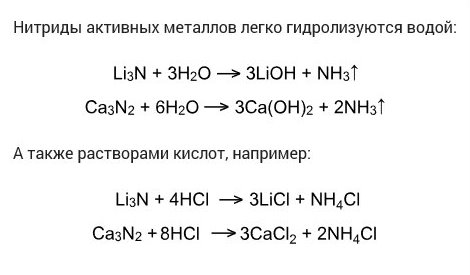
Взаимодействие со сложными веществами.
Реагирует только с гидридами активных металлов:
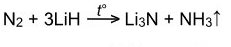
ХИМИЧЕСКИЕ СВОЙСТВА ФОСФОРА
Взаимодействие с неметаллами.
· С кислородом:
При избытке кислорода:
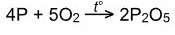
При недостатке кислорода:
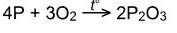
· С галогенами (см. выше)
· С водородом, в отличии от азота, не реагирует!!!
Взаимодействие с металлами
При нагревании реагирует с активными и металлами средней активности. При этом образуются фосфиды:
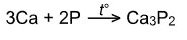

Взаимодействие со сложными веществами
· Фосфор окисляется концентрированными серной и азотной кислотами до ортофосфорной кислоты:
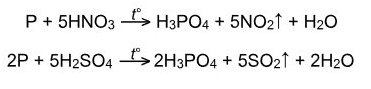
· Диспропорционирует с щелочами на холоду:
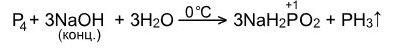
А при кипячении образуется фосфит и выделяется водород:
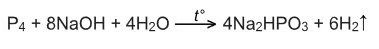
ХИМИЧЕСКИЕ СВОЙСТВА УГЛЕРОДА
У углерода несколько алллотропных модификаций- это алмаз( самая инертная), графит, фуллерен и карбин. Древесный уголь и сажа представляют собой аморфный углерод, и с химической точки зрения является наиболее активной формой углерода.
Углерод способен проявлять восстановительные и окислительные свойства.
Дата: 2018-12-21, просмотров: 437.