Онкотическое и осмотическое давление - сила, с которой молекулы органического и неорганичеcкого вещества притягивают к себе молекулу воды для создания водной оболочки. Осмотическое давление создают вещества неорганической природы, онкотическое - органической.
При общем осмотическом давлении плазмы 7,6 атм, онкотическое давление равно 0,03-0,04 атм (25-30 мм рт. ст.). Крупномолекулярные белки не проникают в интерстициальное пространство из сосудистого русла и являются фактором, определяющим обратный ток воды из межклеточного пространства в венулярном отделе микроциркуляторного русла. Осмотическое и онкотическое давление определяют объемное распределение воды между клеткой и внеклеточным пространством. Вода перемещается через мембрану в сторону более высокого осмотического давления. По величине осмотического давления (основная роль в поддержании которого на 80% принадлежит NaCl, на 15% глюкозе и на 5% мочевине) относительно плазмы все растворы можно разделить на:
1. Изотонические - равные по осмотическому давлению (0,9% раствор NaCl).
2. Гипотонические - с более низким по отношению к плазме осмотическим давлением.
3. Гипертонические - с превышающим осмотическое давление плазмы. Все инъекционные растворы должны быть изотоничными клетке, иначе могут вызвать или потерю воды клеткой (гипертонические растворы), или поступление воды в клетку с последующим ее набуханием и разрывом мембраны (гипотонические растворы).
Кислотно-основное состояние крови. Буферные системы. Алкалоз и ацидоз
Кислотно-основное состояние крови зависит от концентрации в среде ионов водорода, которое выражается в единицах рН . Концентрация водородных ионов (рН = -lg [ Н+] на уровне 7,37 - 7,43 для артериальной крови является жёсткой константой организма. рН венозной крови в связи с более высокой концентрацией углекислого газа и органических кислот ниже и снижается до 7,30 - 7,35, внутриклеточный рН равняется 7,26 - 7,30. Повышение концентрации водородных ионов (снижение рН) определяется как ацидоз, а снижение концентрации протонов обозначается как алкалоз. Сохранение постоянства рН крови обеспечивается физико-химическими буферными системами и функционированием физиологических систем организма - выделительной и дыхания.
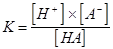 (1)
(1)
Любая буферная система состоит из равновесного соотношения протонов (Н+), сопряжённого основания (А-) и недиссоциированной слабой кислоты: В соответствии с законом действующих масс повышение содержания протонов сопровождается увеличением концентрации недиссоциированной кислоты, а ощелачивание среды приводит к росту диссоциации кислоты с образованием протонов, и константа диссоциации (равновесия) К не изменяется.
Физико-химические буферные системы крови
1. Буферная система гемоглобина является наиболее мощной. Эта система функционирует благодаря тому, что белок глобин в молекуле гемоглобина обладает амфотерными свойствами, оксигемоглобин является более сильной кислотой, чем дезоксигемоглобин (восстановленный гемоглобин). В тканях гемоглобин играет роль щёлочи, в лёгких же ведёт себя как кислота, предотвращая защелачивание крови после выделения из неё углекислоты.
2. Карбонатная буферная система представлена слабой угольной кислотой (Н2СО3) и слабым основанием (NaHCO3-). При поступлении в кровь более сильной, чем угольная, кислоты происходит обмен ионами натрия с образованием слабодиссоциирующей и легкорастворимой угольной кислоты, её избыток снижается при выделении лёгкими углекислого газа.
3. Фосфатная буферная система образована дигидрофосфатом и гидрофосфатом натрия: NаН2РО4/Nа2НРО4. При поступлении в кровь кислоты она реагирует с гидрофосфатом с образованием дигидрофосфата, щёлочь реагирует с дигидрофосфатом натрия, образуя гидрофосфат. В обоих случаях избытки образующихся гидро- или дигидрофосфатов удаляется из организма почками.
4. Белки плазмы играют роль буферной системы благодаря амфотерным свойствам, которые обусловлены амино- и карбоксильной группами: в кислой среде белки ведут себя как щёлочи, связывая кислоты, в щелочной - как кислоты.
Роль функциональных систем. Помимо буферных систем, обеспечивающих базовый уровень регуляции реакции крови, система поддержания рН включает функциональные системы, благодаря которым происходит регенерация буферов.
1. Дыхательная система обеспечивает выделение из организма летучего ангидрида угольной кислоты - углекислого газа.
2. Почки удаляют из организма избыток кислот и оснований. При ацидозе возрастает выделение дигидрофосфата натрия NaН2РО4, при алкалозе - гидрофосфата натрия и NаНСО3, соответственно изменяется кислотность мочи, рН которой колеблется в широком диапазоне (4,5 - 8,5).
3. Важную роль в поддержании рН крови играет желудочно-кишечный тракт, слизистые оболочки которого секретируют эквимолярные количества соляной кислоты (желудок) и гидрокарбоната (кишечник и поджелудочная железа). При патологии состояния, сопровождающиеся неукротимой рвотой, способны привести к алкалозу за счет потери ионов водорода, а поносы, сопровождающиеся потерей бикарбонатов, - к системному ацидозу.
4. Кроме того, в организме функционирует система метаболической нейтрализации - связывания кислых продуктов в процессе аммониогенеза и цикла Карно в печени и почках; а также удаления щелочных валентностей за счет образования молочной кислоты в мышцах.
Белки крови и их значение
1. Обеспечивают онкотическое давление плазмы.
2. Обеспечивают вязкость плазмы, что имеет значение в поддержании артериального давления крови. Вязкость плазмы по отношению к вязкости воды равна 2,2 (1,9-2,6).
3. Белки плазмы играют питательную функцию, являяcь источником аминокислот для клеток (в 3л плазмы содержится около 200 г белков, которые обновляются за 5 суток примерно на 50%).
4. Служат переносчиками гормонов, являются транспортной формой микроэлементов, могут связывать катионы плазмы, препятствуя их потере из организма.
5. Принимают участие в свёртывании крови, являются обязательным компонентом иммунной системы организма, обеспечивают взвешенное состояние эритроцитов, играют роль в поддержании кислотно-основного состояния крови.
Белки плазмы методом электрофореза могут быть разделены на 3 группы: альбумины, глобулины и фибриноген; фракция глобулинов разделяется на альфа-1, альфа-2, бета и гамма-глобулины. Альбумины составляют 60% всех белков плазмы, благодаря низкому молекулярному весу (69000 Д) обеспечивают на 80% онкотическое давление. Благодаря большой суммарной площади поверхности, выполняют роль переносчика многих эндогенных (билирубин, желчные кислоты, соли желчных кислот) и экзогенных веществ. Глобулины образуют комплексные соединения с углеводами, липидами, полисахаридами, связывают гормоны, микроэлементы. Фракция гамма-глобулинов включает иммуноглобулины, агглютинины, многие факторы системы свертывания крови. Фибриноген является источником фибрина, который обеспечивает образования сгустка крови.
Эритроциты, гемоглобин
Эритроциты - безъядерные клетки, основной функцией которых является обеспечение газообмена. 95% массы эритроцитов составляет гемоглобин. Содержание эритроцитов в периферической крови колеблется около 5 млн в 1 мкл. У женщин содержание эритроцитов примерно на 10% ниже, чем у мужчин. Размеры эритроцитов: диаметр 7-8 мкм, объём 85-90 мкм3, площадь поверхности 145 мкм2. Основным источником энергии в эритроцитах является глюкоза, которая на 90% окисляется в ходе анаэробного гликолиза. Энергия расходуется на восстановление текучести мембраны, остаточной деформации, работу ионных насосов, синтез глютатиона в реакциях восстановления, защищающих эритроциты от окислительной денатурации. Синтезируемый в эритроцитах 2,3-дифосфоглицерат (2,3-ДФГ) регулирует (уменьшает) сродство гемоглобина к кислороду, что ускоряет процесс отдачи кислорода. Продолжительность жизни эритроцита 60-90, максимально 120 дней. Разрушение происходит, в основном, макрофагами селезёнки и костного мозга, купферовскими клетками печени (внутриклеточный, внесосудистый гемолиз). После отщепления от гемоглобина гем превращается в желчный пигмент билирубин и поступает в кишечник. Частично всасывается, частично выводится из организма в виде стеркобилина (кал) и уробилина (моча). Железо используется для повторного синтеза гемоглобина. Гемоглобин связывается в крови с белком гаптоглобином, этот комплекс в дальнейшем фагоцитируется купферовскими клетками печени.
Подсчет числа эритроцитов.
Кровь разводится 3% раствором хлорида натрия в 200 раз. Заполняется камера Горяева, под микроскопом подсчитывают число эритроцитов в 5 больших квадратах, расположенных по диагонали счетной камеры. Расчет по формуле :
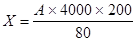 (2).
(2).
X - число эритроцитов;
А - число эритроцитов в 5 больших квадратах (= 80 маленьких);
200 - разведение;
1/4000 мм3 - объём части камеры над 1 маленьким квадратиком;
А/80 - среднее арифметическое число эритроцитов в маленьком квадрате.
Гемоглобин.
Гемоглобин - хромопротеид, окрашенный в красный цвет после присоединения к Fe++ кислорода. Состоит из белка глобина и простетической группы гема. В молекуле гемоглобина содержится одна молекула глобина и четыре молекулы гема. Гем имеет в своем составе атом двухвалентного железа, способный присоединить и отдать молекулу кислорода. Одна молекула гемоглобина присоединяет четыре молекулы кислорода. 1 гр гемоглобина присоединяет 1,34 мл кислорода. Содержание гемоглобина у мужчин 16,6 г в 100 мл крови (166 г/л), у женщин - 130 г/л.
Значение гемоглобина:
1) Выполняет роль переносчика О2 от лёгких к тканям.
2) Участвует в транспорте СО2 от клеток к лёгким.
3) Составляет гемоглобинную буферную систему и регулирует кислотно-основное состояние крови.
Виды гемоглобина
В период внутриутробного развития зародыша (7-12 недель) эритроциты содержат примитивный гемоглобин (HbP), на 9-й неделе появляется гемоглобин фетальный HbF, а перед рождением - гемоглобин взрослых (HbА). Фетальный гемоглобин в течение первого года жизни ребенка полностью заменяется на HbА. Примитивный и фетальный гемоглобины обладают более высоким сродством к кислороду, что обеспечивает его насыщение кислородом при более низком парциальном давлении.
Соединения гемоглобина
В норме гемоглобин содержится в виде нескольких соединений:
1) Восстановленный, или дезоксигемоглобин (Hb). Имеет 4 свободных связи, к которым могут присоединяться лиганды - кислород, угарный газ.
2) Оксигемоглобин (HbО2). Образуется из восстановленного гемоглобина присоединением кислорода.
3) Карбгемоглобин (HbСО2). Образуется в тканях после присоединения к гемоглобину углекислого газа.
Примерно 8-9% гемоглобина в крови находится в виде соединения метгемоглобин (MetHb). Метгемоглобин образуется в результате взаимодействия со свободными радикалами. Железо в метгемоглобине находится в трехвалентной форме, поэтому метгемоглобин не способен взаимодействовать с кислородом.
При отравлениях угарным газом образуется карбоксигемоглобин (HbСО). Обладает высоким сродством к кислороду, поэтому при небольших концентрациях угарного газа в крови гемоглобин блокируется и теряет способность транспортировать кислород.
Определение содержания гемоглобина в крови
Пипеткой набирают 20 мм3 крови и смешивают с 0,1 нормальным раствором соляной кислоты, налитым в среднюю пробирку гемометра Сали. После образования солянокислого гематина - соединения, имеющего интенсивный коричневый цвет, в пробирку по каплям прибавляют дистиллированную воду до уравновешивания цвета раствора в средней пробирке с цветом эталонных растворов. По нанесенной на пробирку шкале по уровню полученного раствора определяют концентрацию гемоглобина.
Гемолиз эритроцитов, виды гемолиза.
Гемолиз - это массивное внутрисосудистое разрушение эритроцитов с выходом свободного гемоглобина в плазму. Гемоглобин начинает выделяться почками, что повреждает нефрон. Виды гемолиза:
1. Осмотический.
2. Химический.
3. Механический.
4. Термический.
5. Биологический.
Причины гемолиза в организме:
1. Переливание несовместимой крови.
2. Сепсис, влияние гемолитических микроорганизмов.
3. Попадание в организм гемолитических ядов.
4. Отравление различными органическими и минеральными веществами.
Опасность гемолиза заключается в развитии комбинированного шока, а в последующем - острой и хронической почечной недостаточности.
Скорость оседания эритроцитов.
При стоянии крови, не свёртывающейся вследствие добавления антикоагулянтов, наблюдается оседание эритроцитов. СОЭ в норме равна у мужчин 1-10 мм/ч, у женщин - 2-15 мм/ч. На СОЭ влияют главным образом свойства плазмы (содержание крупномолекулярных белков - фибриногена и глобулинов), а также размеры и форма эритроцитов. При воспалительных и онкологических заболеваниях скорость оседания эритроцитов возрастает в связи с повышенной способностью эритроцитов образовывать агрегаты. На скорость оседания эритроцитов влияет белковый состав плазмы. СОЭ уменьшается при увеличении содержания альбуминов и возрастает при увеличении концентрации фибриногена, гаптоглобина, липопротеидов, иммуноглобулинов.
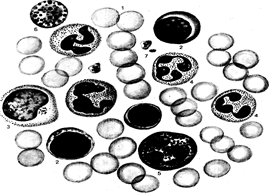
Рис. Клетки периферической крови человека.
1 – эритроциты, 2- лимфоциты, 3- моноциты, 4 – нейтрофильные гранулоциты, 5 – эозинофильные гранулоциты, 6 – базофильные гранулоциты, 7 – тромбоциты.
Дата: 2019-12-10, просмотров: 367.