Характеристика воды
Вода (оксид водорода) — химическое вещество в виде прозрачной жидкости, не имеющей цвета (в малом объёме), запаха и вкуса (при нормальных условиях). Химическая формула: Н2O. В твёрдом состоянии называется льдом или снегом, а в газообразном — водяным паром. Около 71 % поверхности Земли покрыто водой (океаны, моря, озёра, реки, лёд на полюсах).
Вода имеет ключевое значение в создании и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды.
Физические свойства воды
К основным физическим свойствам воды относят цвет, запах, вкус, прозрачность, плотность, сжимаемость, вязкость и электропроводность.
Цвет подземных вод зависит от их химического состава и механических примесей. Обычно подземные воды бесцветны. Желтоватый цвет характерен для вод болотного происхождения, содержащих гуминовые вещества. Сероводородные воды вследствие окисления H2S и образования тонкой коллоидной мути, состоящей из частиц серы, имеют изумрудный оттенок. Цвет воды оценивается по стандартной платино-кобальтовой шкале в градусах.
Запах в подземных водах обычно отсутствует. Ощущение запаха свидетельствует или о наличии газов биохимического происхождения (сероводород и др.), или о присутствии гниющих органических веществ. Характер запаха выражают описательно: без запаха, сероводородный, болотный, гнилостный, плесневелый и т.д. Интенсивность запаха оценивают по шкале в баллах.
Вкус воды зависит от состава растворенных веществ. Соленый вкус вызывается хлористым натрием, горький - сульфатом магния, ржавый - солями железа. Сладковатый вкус имеют воды, богатые органическими веществами, наличие свободной углекислоты придает приятный освежающий вкус. Вкус воды оценивается по таблицам в баллах.
Прозрачность подземных вод зависит от количества растворенных в них минеральных веществ, содержания механических примесей, органических веществ и коллоидов. Для указания степени прозрачности подземных вод служит следующая номенклатура: прозрачная, слабопалесцирующая, опалесцирующая, слегка мутная, мутная, сильно мутная. Мутность воды оценивается в мг\л по стандартной шкале.
Плотность воды определяется отношением ее массы к объему при определенной температуре. За единицу плотности воды принята плотность дистиллированной воды при температуре 4°С. Плотность воды зависит от температуры, количества растворенных в ней солей, газов и взвешенных частиц и изменяется от 1 до 1,4 г/см3.
Сжимаемость воды незначительна и характеризуется коэффициентом сжимаемости β = (2,7-5)10-5 Па. Вязкость воды характеризует внутреннее сопротивление частиц жидкости ее движению, количественно она выражается коэффициентами динамической и кинематической вязкости.
Электропроводность подземных вод зависит от количества растворенных в них солей. Пресные воды обладают незначительной электропроводностью. Дистиллированная вода является изолятором. Электропроводность воды оценивают по удельному электрическому сопротивлению, которое выражается в Ом.м и изменяется от 0,02 до 1,0 Ом.м.
Таблица
| № п/п | Физические константы | Н2О |
| 1 | Молярная масса (г/моль) | 18,015 |
| 2 | Плотность при 20оС | 0,99823 |
| 3 | Температура максимальной плотности, оС | 4 |
| 4 | Температура кипения, оС | 100 |
| 5 | Температура замерзания, оС | 0 |
Химические свойства воды
Химические свойства воды определяются особенностями ее строения. Вода довольно устойчивое вещество, она начинает разлагаться на водород и кислород при нагревании по крайней мере до 1000°С ( происходит термическая диссоциация) или под действием ультрафиолетового излучения (фотохимическая диссоциация). Вода относится к химически активным соединениям. Например, реагирует с фтором. Хлор при нагревании или на свету разлагает воду с выделением атомарного кислорода:
H2O + Cl2 = HCl + HClO (НСlО = НСl + О)
При обычных условиях она взаимодействует с активными металлами:
2H2O + Ca = Ca(ОН)2 + H2
2H2O + 2Na = 2NaOH + H2
Вода вступает в реакцию и со многими неметаллами. Например, при взаимодействии с атомарным кислородом образуется пероксид водорода:
H2O + O = H2O2
Многие оксиды реагируют с водой, образуя основания и кислоты:
CO2 + H2O = H2CO3
CaO + H2O = Ca(OH)2
При взаимодействии с некоторыми солями образуются кристаллогидраты. При нагревании они теряют кристаллизационную воду:
Na2CO3 + 10H2O = Na2CO3 * 10H2O.
Вода также разлагает большинство солей. [1,с.112]
Характеристика фенолов
К фенолам относятся органические соединения с гидроксидной группой в бензольном кольце.
Фенолы присутствуют в бытовых сточных водах и в разнообразных производственных сточных водах химических, нефтеперерабатывающих, нефтехимических, лесохимических, коксохимических, фармацевтических, металлургических, шпалопропиточных, анилинокрасочных и других производств.
В естественных условиях фенолы образуются в процессе метаболизма водных организмов, при биохимическом распаде и трансформации органических веществ.
Фенолы делят на две группы: летучие с паром и нелетучие.
Летучие с паром - это ряд соединений, перегоняющихся с водяным паром.
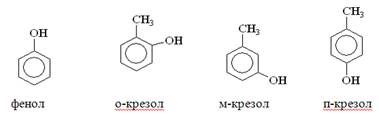
Рис
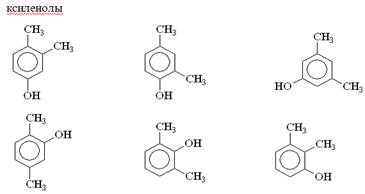
Рис

Рис
Летучие с паром фенолы являются основным компонентом фенольных сточных вод, и вместе с ними они попадают в канализационную сеть и в поверхностные воды, загрязняя их.
Летучие с паром фенолы более токсичные, обладают более интенсивным запахом, чем нелетучие, поэтому допустимые концентрации их в водоемах чрезвычайно малы.
Особенно жесткие требования предъявляются к воде, поступающей на водопроводные станции, где она подвергается обработке хлорированием, потому что хлорпроизводные фенола, О – крезолы, м – крезол имеют неприятный запах даже в самых малых концентрациях.
Для летучих с паром фенолов предельно допустимая концентрация (ПДК) 0,001 мг/л
Нелетучие фенолы
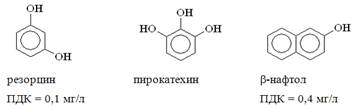
Рис
Так как значения ПДК для разных фенолов различно, то их определяют раздельно.
Физические свойства
Большинство фенолов — бесцветные твердые вещества. Сам фенол плавится при t°=41°C. Присутствие воды в феноле понижает его температуру плавления. Смесь фенола с водой при комнатной температуре — жидкость. Фенол обладает характерным запахом. Если при комнатной температуре фенол растворим в воде незначительно, то при нагревании до 70°С он растворяется полностью.
Фенол — антисептик, его водный раствор используется для дезинфекции и называется карболовой кислотой. Фенол не самый подходящий антисептик, так как вызывает ожоги кожи, а пары его токсичны. Многочисленными исследованиями было установлено, что некоторые замещенные фенолы являются более удобными антисептиками, чем сам фенол. Одно из наиболее употреби-тельных соединений — 2,4,6-трихлорфенол. [2, с.87]
Способы получения фенолов
1. Получение из галогенбензолов. При нагревании хлорбензола и гидроксида натрия под давлением получают фенолят натрия, при дальнейшей обработке которого кислотой образуется фенол:
С6Н5―Сl + 2NaOH → C6H5―ONa + NaCl + Н2О.
2. При каталитическом окислении изопропилбензола (кумола) кислородом воздуха образуются фенол и ацетон:
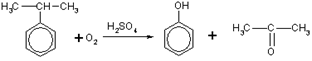
Рис
Это — основной промышленный способ получения фенола.
3. Получение из ароматических сульфокислот. Реакция проводится при сплавлении сульфокислот с щелочами. Первоначально образующиеся феноксиды обрабатывают сильными кислотами для получения свободных фенолов. Метод обычно применяют для получения многоатомных фенолов:
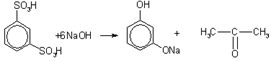
Рис
Влияние на организм
Практически сразу после получения фенола ученые установили, что это химическое вещество обладает не только полезными свойствами, что позволяет его использовать в различных сферах науки и производства, но и является сильнодействующим ядом. Так, вдыхание паров фенола в течение непродолжительного времени может привести к раздражению носоглотки, ожогам дыхательных путей и последующему отеку легких с летальным исходом.
При соприкосновении раствора фенола с кожей образуются химические ожоги, которые впоследствии трансформируются в язвы. Если обработать раствором более 25 процентов кожных покровов, то это может стать причиной смерти человека.
Попадание фенола внутрь организма с питьевой водой, приводит к развитию язвенной болезни, атрофии мышц, нарушению координации движений, кровотечениям.
Кроме этого, ученые установили, что именно фенол является причиной возникновения раковых заболеваний, способствует развитию сердечной недостаточности и бесплодия.
Благодаря свойству окисления, пары этого химического вещества полностью растворяются в воздухе примерно через 20-25 часов. При попадании в почву фенол сохраняет свои ядовитые свойства на протяжении суток. Однако в воде его жизнеспособность может достигать 7-12 дней. Поэтому наиболее вероятный путь попадания этого ядовитого вещества в человеческий организм и на кожные покровы – загрязненная вода. [2, с.89]
Дата: 2019-12-22, просмотров: 439.