Плотность тока выбирается по графику зависимости плотности тока от силы тока для электролизёра заданной мощности. Для данного электролизёра с ВТ в соответствии с графиком плотность тока составляет 0,70А/см2.
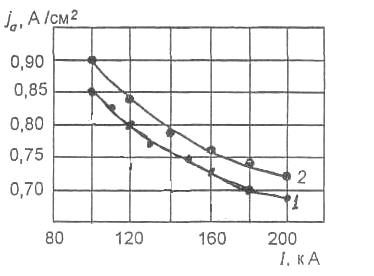
1 - верхний токоподвод; 2 — обожженные аноды.
Расчёт материального баланса
Приход материалов. Рассчитывается по расходу сырья на 1кг алюминия и производительности электролизера в час. Для расчета используем данные, сложившиеся на основании опыта эксплуатации алюминиевых электролизеров.
 Расход сырья (кг/кг AI ) и выход по току (%) для различных типов электролизеров
Расход сырья (кг/кг AI ) и выход по току (%) для различных типов электролизеров
| Материал | Обожженные аноды | Боковой токоподвод | Верхний токоподводд | |
| Глинозем | 1,92-1,93 | 1,92-1,93 | 1,92-1,93 | |
| Аноды, анодная масса | 0,560 | 0,540 | 0,590 | |
| Фториды | 0,052 | 0,045 | 0,090 | |
| В том числе; | ||||
| криолит свежий | 0,011 | 0,030 | 0,019 | |
| криолит регенерационный | 0,015 | | 0,026 | |
| фторид алюминия | 0,025 | 0,020 | 0,043 | |
| фторид кальция | 0,001 | 0,001 | 0,002 | |
| Выход по току | 87-92 | 85-87 | 84-86 | |
Производительность электролизера рассчитываем по формуле:
РАl ═ I×g×hт×10-3, где I- сила тока в амперах,
g-0,3354 г/А.час – электрохимический эквивалент Al,
hт – выход по току (доля единицы)
Задаемся выходом по току (из сложившихся данных- 86%) и вычисляем производительность электролизёра:
РА l = 300000 × 0,3354× 0,86 ×10-3 = 41,824 кг/час
Зная производительность и расход материалов( данные из таблицы), рассчитываем приход материалов:
РAl2O3 ═ рAl2O3 × РАl = 1,93 × 41,824 = 80,72 кг/час – глинозёма;
Ра ═ ра × РАl = = 0,560 × 41,824 = 23,421 кг/ час – анодной массы;
 Ркр.св ═ ркр.св × РАl = 0,011 × 41,824 = 0,460 кг/час – криолита свежего;
Ркр.св ═ ркр.св × РАl = 0,011 × 41,824 = 0,460 кг/час – криолита свежего;
Ркр.рег ═ ркр.рег × РАl = 0,015 × 41,824 =0,627 кг/час – криолита регенерационного;
Рф.ал. ═ рф.ал × РАl = 0,025 × 41,824 =1,046 кг/час – фторида алюминия;
Рф.кал.. ═ рф.кал × РАl = 0,001 × 41,824 =0,042 кг/час – фторида кальция.
Вычислим расход материалов:
Алюминий. Количество полученного алюминия определяется производительностью ванн:
РА l = 46,151 кг/час
Анодные газы.
Количество анодных газов рассчитывают, исходя из их состава и суммарной реакции по формуле: Al 2 O 3 + XC = 2 Al + (3- X ) CO 2 + (2 X - 3) CO, где Х – объёмное содержание СО2 в процентах.
Мольные доли газов определяем из формулы:
N СО2 =2 ( h т - 50), где hT – выход по току.
N СО2 = 2 × ( 86 - 50) = 72 % = 0,72
N СО = 100 – 72= 28%=0,28
Количество СО2 и СО (кмоль/час) определяем по формулам:
Мсо═ N со РА l /[18(2- N со)]
Мсо2 ═ N со2РА l / [18(1+ N со2)]
Мсо= 0,28 ×41,824/ 18(2-0,28)=11,711/30,96= 0,378 кмоль/час
Мсо2 = 0,72×41,824/ 18(1+0,72)=30,113/30,96=0,973 кмоль/час
Рассчитаем весовые количества СО2 и СО (кг/час)
Рсо = 28× 0,378=10,584 кг/час
Рсо2 = 44× 0,973=42,812 кг/час, где 28 – молекулярная масса СО,
44 – молекулярная масса СО2
Потери углерода.
▲Рс═ Ра - Рс ,где Ра- приход анодной массы или обожжённых анодов,
Рс – количество углерода, израсходованного с газами.
 Рс ═12×(Мсо + Мсо2)=12×(0,378+0,973)=12 ×1,315= 15,78 кг/час
Рс ═12×(Мсо + Мсо2)=12×(0,378+0,973)=12 ×1,315= 15,78 кг/час
▲Рс=23,421 – 15,78 = 7,641кг/час
Потери глинозема.
▲ PAl 2 O 3═ PAl 2 O 3 – PAl2O3(теор),где PAl 2 O 3—приход глинозёма в электролизёр, а PAl2O3(теор) – теоретический расход глинозёма.
РAl2O3(теор)═102РАl/54═102×41,824/54=4266,048/54=79,001 (кг/час), где:
54- молекулярная масса алюминия
102- молекулярная масса глинозема
▲ РAl2O3 = 80,72- 79,001 = 1,719 кг/час
Потери фторидов : принимаются равными приходу.
Таб. Материальный баланс
| Приход | Един. изм. кг/час | Расход | Един. изм. кг/час |
| Глинозем, РАl2O3 | 80,72 | Получено алюминия, РА l | 41,824 |
| Криолит свежий, Ркр | 0,460 | Получено со, Рсо | 10,584 |
| Фторид алюминия, Рф.ал. | 1,046 | Получено со2, Рсо2 | 42,812 |
| Фторид кальция, Рф.кал | 0,042 | Криолит свежий, Ркр | 0,460 |
| Криолит регенерационный, Ркр.рег. | 0,627 | Фторид алюминия, Рф.ал. | 1,046 |
| Анодная масса(аноды), Ра | 23,421 | Фторид кальция, Рф.кал | 0,042 |
|
|
| Криолит регенерационный, Ркр.рег | 0,627 |
| Потери углерода, ▲Рс | 7,641 | ||
| Потери глинозема, ▲ РАl2O3 | 1,719 | ||
| ИТОГО | 106,316 | ИТОГО | 97,755 |
 Конструктивный расчёт.
Конструктивный расчёт.
Конструктивный расчёт электролизёра необходим для определения его основных размеров.
Определение площади анода.
По заданной силе тока 300000 А и выбранной в соответствии графиком зависимости анодной плотности тока от силы тока, величины плотности тока - 0,70 А/см2, определим площадь анода по формуле:
J=l/S , откуда : S а = I/ja ;
S = 300000А : 0,70А/см2= 207142,85 см2
Дата: 2019-12-22, просмотров: 325.
