КСЕ
Химические закономерности.
Гомогенные и гетерогенные системы.
Под химической системой можем понимать одно или несколько веществ, отделенных от внешней среды воображаемой или реальной границей.
Гомогенные системы – система, обладающая на всем протяжении одинаковым химическим составом, одинаковыми химическими и физическими свойствами (воздух, спирт, вода).
Гетерогенная система – система, состоящая из двух или нескольких частей, различающихся по своим физическим или химическим свойствам и отделенных друг от друга поверхностями раздела (вода и оксид алюминия).
Энергетические эффекты химических реакций.
Эндотермическая реакция (поглощение тепла)
Экзотермическая реакция (выделение тепла)
Люминесцентное свечение – выделение «холодного» света
Закон Гесса.
«Тепловой эффект реакции зависит только от начального и конечного состояния веществ и не зависит от промежуточных стадий процесса»
Скорость химических реакций.
Под скоростью хим. Реакции мы понимаем изменение концентрации любого из исходных или образующихся веществ за короткий промежуток времени (мгновенная скорость)
Мгновенная и средняя скорость реакции.
Теория активированного комплекса.
Развитие квантовой механики привело к созданию теории активирован-
ного комплекса (переходного состояния), предложенной в 1935 году одновре-
менно Эйрингом, Эвансом и Поляни. Но первые основные идеи теории были сформулированы Р. Марселинов в 1915 г.
Энергия активации.
Энергия активации – минимальная энергия необходимая для протекания хим. Реакции активированного комплекса
Закон действующих масс и факторы, влияющие на скорость реакции.
Закон действующих масс (основное уравнение кинетики) устанавливает соотношение между массами реагирующих веществ в химических реакциях при равновесии. Закон действующих масс сформулирован в 1864—1867 гг. К. Гульдбергом и П. Вааге. Согласно этому закону при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ.
Закон действующих масс используют при различных расчетах химических процессов. Он позволяет решить вопрос, в каком направлении возможно самопроизвольное течение рассматриваемой реакции при заданном соотношении концентраций реагирующих веществ, какой выход нужного продукта может быть получен.
Скорость химической реакции зависит от концентрации реагентов, температуры, катализатора, природы реагирующих веществ.
t , присутствия катализаторов, а также от некоторых других факторов (например, от давления - для газовых реакций, от измельчения - для твердых веществ, от радиоактивного облучения).
Влияние концентраций реагирующих веществ. Чтобы осуществлялось химическое взаимодействие веществ А и В, их молекулы (частицы) должны столкнуться. Чем больше столкновений, тем быстрее протекает реакция. Число же столкновений тем больше, чем выше концентрация реагирующих веществ. Отсюда на основе обширного экспериментального материала сформулирован основной закон химической кинетики, устанавливающий зависимость скорости реакции от концентрации реагирующих веществ:
Cкорость химической реакции пропорциональна произведению концентраций реагирующих веществ.
Для реакции ( I ) этот закон выразится уравнением
v = kcA cB , (1)
где сА и сВ - концентрации веществ А и В, моль/л; k - коэффициент пропорциональности, называемый константой скорости реакции. Основной закон химической кинетики часто называют законом действующих масс.
Из уравнения (1) нетрудно установить физический смысл константы скорости k : она численно равна скорости реакции, когда концентрации каждого из реагирующих веществ составляют 1 моль/л или когда их произведение равно единице.
Константа скорости реакции k зависит от природы реагирующих веществ и от температуры, но не зависит от их концентраций.
Уравнение (1), связывающее скорость реакции с концентрацией реагирующих веществ, называется кинетическим уравнением реакции. Если опытным путем определено кинетическое уравнение реакции, то с его помощью можно вычислять скорости при других концентрациях тех же реагирующих веществ.
Влияние температуры .
Зависимость скорости реакции от температуры определяется правилом Вант-Гоффа:
При повышении температуры на каждые 10о скорость большинства реакций увеличивается в 2-4 раза.
Математически эта зависимость выражается соотношением
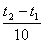
vt 2 = vt 1 γ ,
где vt 1 , vt 2 - скорости реакции соответственно при начальной ( t 1 ) и конечной ( t 2 ) температурах, а γ - температурный коэффициент скорости реакции, который показывает, во сколько раз увеличивается скорость реакции с повышением температуры реагирующих веществ на 10°.
Правило Вант-Гоффа является приближенным и применимо лишь для ориентировочной оценки влияния температуры на скорость реакции. Температура влияет на скорость химической реакции, увеличивая константу скорости.
Явление катализа.
- явление изменения скорости химической или биохимической реакции в присутствии веществ (катализаторов или ингибиторов), которые многократно вступают в промежуточные взаимодействия и восстанавливаются после цикла реакций.
Химия катализа изучает вещества, изменяющие скорость химических реакций. Вещества, замедляющие реакции, называются ингибиторами. Ферменты — это биологические катализаторы. В присутствии катализаторов, энергия активации уменьшается, скорость хим. реакции увеличивается. Катализатор – вещество, которое участвует в химической реакции, но оставляет после реакции свою первоначальную форму.
Необратимые и обратимые реакции.
Реакции, которые протекают только в одном направлении и завершаются полным превращением исходных реагирующих веществ в конечные вещества, называются необратимыми.
Обратимыми называются такие реакции, которые одновременно протекают в двух взаимно противоположных направлениях.
Химическое равновесие.
- состояние обратимой реакции, когда скорость прямой и обратной реакции равны между собой. Химическое равновесие – состояние динамическое, реакция не прекращается; скорость изменения концентраций исходных веществ в единицу времени равна скорости изменения концентраций образующихся веществ в единицу времени. Т. о. с наступлением хим. равновесия концентрации участников реакции приобретают постоянное значение и не изменяются с течением времени, если не меняются условия протекания реакции.
Смещение химического равновесия и принцип Ле Шателье.
Влияние внешних условий на состояние химического равновесия описывается принципом Ле Шателье: если на систему, находящуюся в состоянии химического равновесия, оказать какое-либо воздействие, то равновесие смещается в сторону реакции, уменьшающей оказанное воздействие:
1) Увеличение концентрации реагентов приводит к смещению равновесия вправо и наоборот;
2) Повышение температуры приводит к смещению равновесия в сторону эндотермической реакции;
3) Повышение давления приводит к смещению равновесия в сторону меньшего числа молекул (только для газофазных реакций).
Зарождение жизни на Земле.
Гипотезы зарождения жизни: креационизм, панспермия, вечного существования и самозарождения.
Креационизм (от англ. creation — создание) — религиозно-философская концепция, в рамках которой всё многообразие органического мира, человечества, планеты Земля, а также мир в целом, рассматриваются как намеренно созданные неким верховным существом или божеством. Теория креационизма, отсылая ответ на вопрос о возникновении жизни к религии (сотворение жизни Богом), по критерию Поппера находится вне поля научных изысканий (так как она неопровержима: научными методами невозможно доказать, как то, что Бог не сотворял жизни, так и то, что Бог ее сотворял). Кроме того, эта теория не дает удовлетворительного ответа на вопрос о причинах возникновения и существования самого верховного существа, обычно просто постулируя его безначальность.
Панспермия— гипотеза о появлении жизни на Земле в результате переноса с других планет каких-либо «зародышей жизни». Согласно панспермии, рассеянные в мировом пространстве зародыши жизни (например, споры микроорганизмов) переносятся с одного небесного тела на другое с метеоритами или под действием давления света. С помощью панспермии объясняли и появление жизни на Земле. После открытия космических лучей и выяснения действия радиации на биологические объекты позиция гипотезы весьма ослабла.
Согласно теории стационарного состояния, Земля никогда не возникала, а существовала вечно; она всегда была способна поддерживать жизнь, а если и изменялась, то очень незначительно. Согласно этой версии, виды также никогда не возникали, они существовали всегда, и у каждого вида есть лишь две возможности — либо изменение численности, либо вымирание.
Эта теория была распространена в Древнем Китае, Вавилоне и Древнем Египте в качестве альтернативы креационизму, с которым она сосуществовала. Аристотель (384—322 гг. до н. э.), которого часто провозглашают основателем биологии, придерживался теории спонтанного зарождения жизни. Согласно этой гипотезе, определенные «частицы» вещества содержат некое «активное начало», которое при подходящих условиях может создать живой организм. Аристотель был прав, считая, что это активное начало содержится в оплодотворенном яйце, но ошибочно полагал, что оно присутствует также в солнечном свете, тине и гниющем мясе.
С распространением христианства теория спонтанного зарождения жизни оказалась не в чести, но эта идея все продолжала существовать где-то на заднем плане в течение еще многих веков.
Абиогенная теория зарождения жизни: отбор химических элементов, отбор соединений, катализаторов и химических систем, способных к самовоспроизводству.
Теория химической эволюции или пребиотическая эволюция — первый этап эволюции жизни, в ходе которого органические, пребиотические вещества возникли из неорганических молекул под влиянием внешних энергетических и селекционных факторов и в силу развертывания процессов самоорганизации, свойственных всем относительно сложным системам, которыми бесспорно являются все углерод-содержащие молекулы.
Основу живых систем составляют только шесть элементов, получивших название органогенов: углерод, водород, кислород, азот, фосфор, сера, общая весовая доля которых в организме составляет более 97%. За ними следуют 11 элементов, которые участвуют в построении физиологически важных компонентов биосистем: натрий, калий, кальций, магний, железо, кремний, алюминий, хлор, медь, цинк, кобальт. Их весовая доля в организме – 1,6%. Есть еще 20 элементов, участвующих в построении и функционировании отдельных узкоспецифических биосистем, доля которых составляет около 1%. Отбор химических соединений – устойчивые и лобильные ( при минимальных затратах энергии)
Химическая эволюция и роль фосфорных соединений и РНК.
ЧЕЛОВЕК - биосоциальное существо, т. е. живое существо, обладающее даром мышления и речи, нравственно-этическими качествами, способностью создавать орудия труда и пользоваться ими в процессе общественного производства; субъект исторического процесса, творец всей материальной и духовной культуры.
КСЕ
Химические закономерности.
Гомогенные и гетерогенные системы.
Под химической системой можем понимать одно или несколько веществ, отделенных от внешней среды воображаемой или реальной границей.
Гомогенные системы – система, обладающая на всем протяжении одинаковым химическим составом, одинаковыми химическими и физическими свойствами (воздух, спирт, вода).
Гетерогенная система – система, состоящая из двух или нескольких частей, различающихся по своим физическим или химическим свойствам и отделенных друг от друга поверхностями раздела (вода и оксид алюминия).
Энергетические эффекты химических реакций.
Эндотермическая реакция (поглощение тепла)
Экзотермическая реакция (выделение тепла)
Люминесцентное свечение – выделение «холодного» света
Закон Гесса.
«Тепловой эффект реакции зависит только от начального и конечного состояния веществ и не зависит от промежуточных стадий процесса»
Скорость химических реакций.
Под скоростью хим. Реакции мы понимаем изменение концентрации любого из исходных или образующихся веществ за короткий промежуток времени (мгновенная скорость)
Мгновенная и средняя скорость реакции.
Теория активированного комплекса.
Развитие квантовой механики привело к созданию теории активирован-
ного комплекса (переходного состояния), предложенной в 1935 году одновре-
менно Эйрингом, Эвансом и Поляни. Но первые основные идеи теории были сформулированы Р. Марселинов в 1915 г.
Энергия активации.
Энергия активации – минимальная энергия необходимая для протекания хим. Реакции активированного комплекса
Закон действующих масс и факторы, влияющие на скорость реакции.
Закон действующих масс (основное уравнение кинетики) устанавливает соотношение между массами реагирующих веществ в химических реакциях при равновесии. Закон действующих масс сформулирован в 1864—1867 гг. К. Гульдбергом и П. Вааге. Согласно этому закону при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ.
Закон действующих масс используют при различных расчетах химических процессов. Он позволяет решить вопрос, в каком направлении возможно самопроизвольное течение рассматриваемой реакции при заданном соотношении концентраций реагирующих веществ, какой выход нужного продукта может быть получен.
Скорость химической реакции зависит от концентрации реагентов, температуры, катализатора, природы реагирующих веществ.
t , присутствия катализаторов, а также от некоторых других факторов (например, от давления - для газовых реакций, от измельчения - для твердых веществ, от радиоактивного облучения).
Влияние концентраций реагирующих веществ. Чтобы осуществлялось химическое взаимодействие веществ А и В, их молекулы (частицы) должны столкнуться. Чем больше столкновений, тем быстрее протекает реакция. Число же столкновений тем больше, чем выше концентрация реагирующих веществ. Отсюда на основе обширного экспериментального материала сформулирован основной закон химической кинетики, устанавливающий зависимость скорости реакции от концентрации реагирующих веществ:
Cкорость химической реакции пропорциональна произведению концентраций реагирующих веществ.
Для реакции ( I ) этот закон выразится уравнением
v = kcA cB , (1)
где сА и сВ - концентрации веществ А и В, моль/л; k - коэффициент пропорциональности, называемый константой скорости реакции. Основной закон химической кинетики часто называют законом действующих масс.
Из уравнения (1) нетрудно установить физический смысл константы скорости k : она численно равна скорости реакции, когда концентрации каждого из реагирующих веществ составляют 1 моль/л или когда их произведение равно единице.
Константа скорости реакции k зависит от природы реагирующих веществ и от температуры, но не зависит от их концентраций.
Уравнение (1), связывающее скорость реакции с концентрацией реагирующих веществ, называется кинетическим уравнением реакции. Если опытным путем определено кинетическое уравнение реакции, то с его помощью можно вычислять скорости при других концентрациях тех же реагирующих веществ.
Влияние температуры .
Зависимость скорости реакции от температуры определяется правилом Вант-Гоффа:
При повышении температуры на каждые 10о скорость большинства реакций увеличивается в 2-4 раза.
Математически эта зависимость выражается соотношением
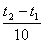
vt 2 = vt 1 γ ,
где vt 1 , vt 2 - скорости реакции соответственно при начальной ( t 1 ) и конечной ( t 2 ) температурах, а γ - температурный коэффициент скорости реакции, который показывает, во сколько раз увеличивается скорость реакции с повышением температуры реагирующих веществ на 10°.
Правило Вант-Гоффа является приближенным и применимо лишь для ориентировочной оценки влияния температуры на скорость реакции. Температура влияет на скорость химической реакции, увеличивая константу скорости.
Явление катализа.
- явление изменения скорости химической или биохимической реакции в присутствии веществ (катализаторов или ингибиторов), которые многократно вступают в промежуточные взаимодействия и восстанавливаются после цикла реакций.
Химия катализа изучает вещества, изменяющие скорость химических реакций. Вещества, замедляющие реакции, называются ингибиторами. Ферменты — это биологические катализаторы. В присутствии катализаторов, энергия активации уменьшается, скорость хим. реакции увеличивается. Катализатор – вещество, которое участвует в химической реакции, но оставляет после реакции свою первоначальную форму.
Необратимые и обратимые реакции.
Реакции, которые протекают только в одном направлении и завершаются полным превращением исходных реагирующих веществ в конечные вещества, называются необратимыми.
Обратимыми называются такие реакции, которые одновременно протекают в двух взаимно противоположных направлениях.
Химическое равновесие.
- состояние обратимой реакции, когда скорость прямой и обратной реакции равны между собой. Химическое равновесие – состояние динамическое, реакция не прекращается; скорость изменения концентраций исходных веществ в единицу времени равна скорости изменения концентраций образующихся веществ в единицу времени. Т. о. с наступлением хим. равновесия концентрации участников реакции приобретают постоянное значение и не изменяются с течением времени, если не меняются условия протекания реакции.
Смещение химического равновесия и принцип Ле Шателье.
Влияние внешних условий на состояние химического равновесия описывается принципом Ле Шателье: если на систему, находящуюся в состоянии химического равновесия, оказать какое-либо воздействие, то равновесие смещается в сторону реакции, уменьшающей оказанное воздействие:
1) Увеличение концентрации реагентов приводит к смещению равновесия вправо и наоборот;
2) Повышение температуры приводит к смещению равновесия в сторону эндотермической реакции;
3) Повышение давления приводит к смещению равновесия в сторону меньшего числа молекул (только для газофазных реакций).
Геологическая история и строение Земли.
Образование солнечной системы.
Согласно современным представлениям, формирование Солнечной системы началось около 4,6 млрд лет назад с гравитационного коллапса небольшой части гигантского межзвёздного молекулярного облака. Большая часть вещества оказалась в гравитационном центре коллапса с последующим образованием звезды — Солнца. Вещество, не попавшее в центр, сформировало вращающийся вокруг него протопланетный диск, из которого в дальнейшем сформировались планеты, их спутники, астероиды и другие малые тела Солнечной системы.
Формирование и геологическая эволюция Земли.
Геологическое строение Земли: атмосфера, литосфера, биосфера.
Атмосфера — газовая оболочка, окружающая планету Земля. Совокупность разделов физики и химии, изучающих атмосферу, принято называть физикой атмосферы. Атмосфера определяет погоду на поверхности Земли, изучением погоды занимается метеорология, а длительными вариациями климата — климатология.
Азот – 78,084 %, Кислород – 20,946 %, другие газы…
1) Тропосфера ( 8 – 18 км) нижний основной слой атмосферы
2) Стратосфера (11 – 50 км)
3) Мезосфера (50 – 90 км)
4) Термосфера (200 – 800 км)
5) Экзосфера — зона рассеяния, внешняя часть термосферы, расположенная выше 700 км. Газ в экзосфере сильно разрежен, и отсюда идёт утечка его частиц в межпланетное пространство (диссипация).
Литосфе́ра (от греч. λίθος — камень и σφαίρα — шар, сфера) — твёрдая оболочка Земли. Состоит из земной коры и верхней части мантии, до астеносферы, где скорости сейсмических волн понижаются, свидетельствуя об изменении пластичности пород. В строении литосферы выделяют подвижные области (складчатые пояса) и относительно стабильные платформы.
Биосфе́ра (от греч. βιος — жизнь и σφαῖρα — сфера, шар) — оболочка Земли, заселённая живыми организмами, находящаяся под их воздействием и занятая продуктами их жизнедеятельности; «пленка жизни»; глобальная экосистема Земли.
Зарождение жизни на Земле.
Гипотезы зарождения жизни: креационизм, панспермия, вечного существования и самозарождения.
Креационизм (от англ. creation — создание) — религиозно-философская концепция, в рамках которой всё многообразие органического мира, человечества, планеты Земля, а также мир в целом, рассматриваются как намеренно созданные неким верховным существом или божеством. Теория креационизма, отсылая ответ на вопрос о возникновении жизни к религии (сотворение жизни Богом), по критерию Поппера находится вне поля научных изысканий (так как она неопровержима: научными методами невозможно доказать, как то, что Бог не сотворял жизни, так и то, что Бог ее сотворял). Кроме того, эта теория не дает удовлетворительного ответа на вопрос о причинах возникновения и существования самого верховного существа, обычно просто постулируя его безначальность.
Панспермия— гипотеза о появлении жизни на Земле в результате переноса с других планет каких-либо «зародышей жизни». Согласно панспермии, рассеянные в мировом пространстве зародыши жизни (например, споры микроорганизмов) переносятся с одного небесного тела на другое с метеоритами или под действием давления света. С помощью панспермии объясняли и появление жизни на Земле. После открытия космических лучей и выяснения действия радиации на биологические объекты позиция гипотезы весьма ослабла.
Согласно теории стационарного состояния, Земля никогда не возникала, а существовала вечно; она всегда была способна поддерживать жизнь, а если и изменялась, то очень незначительно. Согласно этой версии, виды также никогда не возникали, они существовали всегда, и у каждого вида есть лишь две возможности — либо изменение численности, либо вымирание.
Эта теория была распространена в Древнем Китае, Вавилоне и Древнем Египте в качестве альтернативы креационизму, с которым она сосуществовала. Аристотель (384—322 гг. до н. э.), которого часто провозглашают основателем биологии, придерживался теории спонтанного зарождения жизни. Согласно этой гипотезе, определенные «частицы» вещества содержат некое «активное начало», которое при подходящих условиях может создать живой организм. Аристотель был прав, считая, что это активное начало содержится в оплодотворенном яйце, но ошибочно полагал, что оно присутствует также в солнечном свете, тине и гниющем мясе.
С распространением христианства теория спонтанного зарождения жизни оказалась не в чести, но эта идея все продолжала существовать где-то на заднем плане в течение еще многих веков.
Абиогенная теория зарождения жизни: отбор химических элементов, отбор соединений, катализаторов и химических систем, способных к самовоспроизводству.
Теория химической эволюции или пребиотическая эволюция — первый этап эволюции жизни, в ходе которого органические, пребиотические вещества возникли из неорганических молекул под влиянием внешних энергетических и селекционных факторов и в силу развертывания процессов самоорганизации, свойственных всем относительно сложным системам, которыми бесспорно являются все углерод-содержащие молекулы.
Основу живых систем составляют только шесть элементов, получивших название органогенов: углерод, водород, кислород, азот, фосфор, сера, общая весовая доля которых в организме составляет более 97%. За ними следуют 11 элементов, которые участвуют в построении физиологически важных компонентов биосистем: натрий, калий, кальций, магний, железо, кремний, алюминий, хлор, медь, цинк, кобальт. Их весовая доля в организме – 1,6%. Есть еще 20 элементов, участвующих в построении и функционировании отдельных узкоспецифических биосистем, доля которых составляет около 1%. Отбор химических соединений – устойчивые и лобильные ( при минимальных затратах энергии)
Химическая эволюция и роль фосфорных соединений и РНК.
Дата: 2019-12-10, просмотров: 365.